处方信息要点
这些重点内容不包括安全有效地使用BALVERSA所需的所有信息。查看BALVERSA的完整处方信息。
BALVERSA ®(erdafitinib)片剂,用于口服的
初步批准美国:2019
适应症和用途
BALVERSA是一种激酶抑制剂,可用于治疗患有局部晚期或转移性尿路上皮癌(mUC)的成年患者,
· 易感FGFR3或FGFR2遗传改变和
· 在至少一系以前的含铂化学疗法期间或之后进展,包括在新辅助或辅助含铂化学疗法的12个月内。
根据FDA批准的BALVERSA伴随诊断选择患者进行治疗。(1,2.1)
该适应症是根据肿瘤反应率在加速批准下批准的。对于该适应症的持续批准可能取决于验证性试验中对临床益处的验证和描述。(1,14)
剂量和给药
· 在开始用BALVERSA治疗之前,确认肿瘤标本中存在FGFR基因改变。(2.1)
· 建议的初始剂量:口服8mg,每天一次,如果符合标准,剂量增加到9 mg,每天。(2.2)
· 整片吞咽。(2.2)
剂量形式和强度
片剂:3 mg,4mg和5 mg。(3)
禁忌症
没有。(4)
警告和注意事项
· 眼部疾病:BALVERSA可引起中央性浆液性视网膜病变/视网膜色素上皮脱离(CSR/ RPED)在治疗的前四个月,此后每三个月以及在任何时候进行视觉检查,每月进行一次眼科检查。发生CSR / RPED时扣留BALVERSA,如果4周内仍未解决或严重性为4级,则永久终止使用BALVERSA。 (2.3,5.1)
· 高磷酸盐血症:磷酸盐水平升高是BALVERSA的药效学作用。监测高磷血症并在需要时调整剂量(2.3,5.2)
· 胚胎胎儿毒性:可引起胎儿伤害。建议的潜在风险对胎儿和患者使用有效的避孕(5.3,8.1,8.3)。
不良反应
最常见的不良反应包括实验室异常(≥20%)为磷酸盐增加,口腔炎,疲劳,肌酐增加,腹泻,口干,小肠分解,丙氨酸氨基转移酶增加,碱性磷酸酶增加,钠减少,食欲下降,白蛋白减少,消化不良,血红蛋白减少,皮肤干燥,天冬氨酸转氨酶增加,镁减少,干眼症,脱发,手掌-足红斑感觉综合症,便秘,磷酸盐减少,腹痛,钙增加,恶心和肌肉骨骼疼痛。(6.1)
要报告可疑的不良反应,请联系Janssen Products,LP。请致电1-800-526-7736(1-800-JANSSEN和www.BALVERSA.com)或FDA请致电1-800-FDA-1088或www.fda.gov/medwatch。
药物相互作用
· 中度CYP2C9或强CYP3A4抑制剂:考虑使用其他药物或密切监测不良反应。(7.1)
· CYP2C9或CYP3A4的强诱导剂:避免与BALVERSA并用。(7.1)
· 中度CYP2C9或CYP3A4诱导剂:将BALVERSA剂量增加至9 mg。(7.1)
· 改变血清磷酸盐水平的试剂:避免在初始剂量调整期之前与可能改变血清磷酸盐水平的试剂同时使用。(2.3,7.1)
· CYP3A4底物:避免与治疗指数狭窄的敏感CYP3A4底物同时使用。(7.2)
· OCT2底物:考虑使用替代剂或根据耐受性考虑减少OCT2底物的剂量。(7.2)
· P-gp底物:在给药具有较窄治疗指数的P-gp底物之前或之后至少6小时分开BALVERSA给药。(7.2)
在特定人口中使用
· 哺乳期:建议不要母乳喂养。(8.2)
有关患者咨询信息和FDA批准的患者标签,请参见17。
完整的处方信息:目录*
1适应症和用途
2剂量和给药
2.1患者选择
2.2推荐剂量和时间表
2.3不良反应的剂量修改
3剂型和强度
4禁忌症
5警告和注意事项
5.1眼部疾病
5.2高磷血症
5.3胚胎-胎儿毒性
6不良反应
6.1临床试验经验
7药物相互作用
7.1其他药物对BALVERSA的影响
7.2 BALVERSA对其他药物的作用
8在特定人群中的使用
8.1怀孕
8.2哺乳
8.3生殖潜力的男性和女性
8.4小儿使用
8.5老年用途
8.6 CYP2C9弱代谢者
11说明
12临床药理学
12.1行动机制
12.2药效学
12.3药代动力学
12.5药物基因组学
13毒理学
13.1致癌,诱变和生育能力受损
14临床研究
14.1具有易感FGFR基因改变的尿道上皮癌
16供应/存储和处理方式
17患者咨询信息
未列出全部处方信息中的节或小节。
完整的处方信息
1适应症和用途
BALVERSA用于治疗患有局部晚期或转移性尿路上皮癌(mUC)的成年患者,其具有:
· 敏感的FGFR3或FGFR2遗传改变,以及
· 在至少一系行先前的含铂化疗期间或之后进展,包括在新辅助或辅助含铂化疗的12个月内。
根据FDA批准的BALVERSA伴随诊断选择患者进行治疗[请参阅剂量和给药方法(2.1)和 临床研究(14) ]。
该适应症是根据肿瘤反应率在加速批准下批准的。继续批准该适应症可能要取决于验证性试验中对临床益处的验证和描述[见临床研究(14) ]。
2剂量和给药
2.1患者选择
根据FDA批准的伴随诊断法检测到的肿瘤标本中存在敏感的FGFR基因改变,选择用于治疗BALVERSA的局部晚期或转移性尿路上皮癌的患者 [参见临床研究(14.1) ]。
有关FDA批准的尿路上皮癌FGFR基因改变检测方法的信息,请访问:http : //www.fda.gov/CompanionDiagnostics。
2.2推荐剂量和时间表
BALVERSA的建议起始剂量为每天口服一次8 mg(两片4 mg片剂),根据血清磷酸盐(PO 4)水平和14至21天的耐受性,剂量应增加到每天一次9 mg(三片3 mg片剂)[参见剂量和给药方法(2.3) ]。
吞咽整个或不带食物的片剂。如果在服用BALVERSA之后的任何时间出现呕吐,则应在第二天服用下一剂。治疗应继续进行,直到疾病进展或出现不可接受的毒性。
如果错过了一定剂量的BALVERSA,可以在同一天尽快服用。第二天恢复BALVERSA的常规每日剂量表。不应服用多余的药片来弥补错过的剂量。
根据血清磷酸盐水平增加剂量
开始治疗后14至21天评估血清磷酸盐水平。如果血清磷酸盐水平<5.5 mg / dL,并且没有眼部疾病或2级以上的不良反应,则每天增加BALVERSA的剂量至9 mg。每月监测高磷酸盐血症的磷酸盐水平[见药效学(12.2) ]。
2.3不良反应的剂量修改
表1列出了建议的不良反应剂量调整方法。
| 表1:BALVERSA减量时间表 | |||||
| 剂量 | 第一次剂量减少 | 2 次剂量减少 | 3 次剂量减少 | 第 4 次减量 | 第 5 次减量 |
| 9毫克⭢ (3毫克3片) | 8毫克 (2片4毫克) | 6毫克 (两片3毫克) | 5毫克 (1毫克5片) | 4毫克 (1毫克4片) | 停止 |
| 8 mg⭢ (两片4 mg片) | 6毫克 (两片3毫克) | 5毫克 (1毫克5片) | 4毫克 (1毫克4片) | 停止 | |
表2总结了在特定不良反应管理中中断,减少或中断BALVERSA的建议。
| 表2:不良反应的剂量修改 | |
| 不良反应 | BALVERSA剂量调整 |
| 高磷血症 | |
| 在所有患者中,将磷酸盐的摄入量限制为每天600-800 mg。如果血清磷酸盐高于7.0 mg / dL,请考虑添加口服磷酸盐结合剂,直到血清磷酸盐水平恢复至<5.5 mg / dL。 | |
| 5.6–6.9 mg / dL(1.8–2.3 mmol / L) | 继续以当前剂量服用BALVERSA。 |
| 7.0–9.0 mg / dL(2.3–2.9 mmol / L) | 每周重新评估BALVERSA,直到水平恢复至<5.5 mg / dL(或基线)。然后以相同的剂量水平重新启动BALVERSA。对于持续> 1周的高磷血症,可降低剂量。 |
| > 9.0 mg / dL(> 2.9 mmol / L) | 每周重新评估BALVERSA,直到水平恢复至<5.5 mg / dL(或基线)。然后可以降低1剂量水平重新启动BALVERSA。 |
| > 10.0 mg / dL(> 3.2 mmol / L)或基线肾功能明显改变或3级高钙血症 | 每周重新评估BALVERSA,直到水平恢复至<5.5 mg / dL(或基线)。然后可以降低2剂量水平重新启动BALVERSA。 |
| 中枢性浆液性视网膜病变/视网膜色素上皮脱离(CSR / RPED) | |
| 1级:无症状;仅临床或诊断意见 | 保留直到解决。如果在4周内解决,请以下一个较低的剂量恢复。然后,如果一个月没有复发,请考虑重新升级。如果连续2次眼科检查稳定,但仍未解决,则以下一个较低的剂量水平恢复。 |
| 2级:视力比基线低20/40或≤3线 | 保留直到解决。如果在4周内解决,可以在下一个较低的剂量水平恢复。 |
| 3级:视力比基线差20/40或> 3线 | 保留直到解决。如果在4周内解决,可以降低两个剂量水平。如果再次发生,请考虑永久终止。 |
| 4级:患眼的视力20/200或更差 | 永久停产。 |
| 其他不良反应* | |
| 3级 | 暂不使用BALVERSA,直到恢复为1级或基线,然后可以恢复较低的剂量水平。 |
| 四级 | 永久停产。 |
*使用美国国家癌症研究所不良事件通用术语标准(NCICTCAEv4.03)对剂量调整进行分级。
3剂型和强度
片剂:
· 3毫克:黄色,圆形双凸,薄膜包衣,一侧凹陷有“ 3”;另一边是“ EF”。
· 4 mg:橙色,圆形双凸,薄膜包衣,在一侧凹陷有“ 4”;另一边是“ EF”。
· 5毫克:褐色,圆形双凸,薄膜包衣,在一侧凹陷有“ 5”;另一边是“ EF”。
4禁忌症
没有。
5警告和注意事项
5.1眼部疾病
BALVERSA可引起眼部疾病,包括中央性浆液性视网膜病变/视网膜色素上皮脱离(CSR / RPED),导致视野缺损。
据报道,在接受BALVERSA治疗的患者中,有25%的患者接受了CSR / RPED,首次发作的中位时间为50天。3%的患者报告了涉及中心视野的3级CSR / RPED。在研究截止时,CSR / RPED在13%的患者中得到解决,并且在13%的患者中正在进行。CSR / RPED导致剂量中断,分别减少9%和14%的患者和3%的停用BALVERSA的患者。
BALVERSA治疗期间28%的患者出现干眼症状,6%的患者出现3级症状。所有患者均应根据需要接受预防性干眼及眼用缓和剂。
在治疗的前4个月和此后每3个月进行每月的眼科检查,并在任何时候紧急检查视觉症状。眼科检查应包括视力评估,裂隙灯检查,眼底镜检查和光学相干断层扫描。
发生CSR时,请暂不使用BALVERSA;如果4周内仍未解决,或严重性为4级,则永久终止使用BALVERSA。对于眼部不良反应,请遵循剂量调整指南[参见剂量和用法(2.3) ]。
5.2高磷血症
磷酸盐水平的升高是BALVERSA的药效学作用[见药效学(12.2) ]。据报道76%的BALVERSA患者有高磷酸盐血症的不良反应。开始BALVERSA治疗后,任何高磷血症分级事件的中位发作时间为20天(范围:8 –116)。BALVERSA治疗期间有32%的患者接受了磷酸盐结合剂。
监控高磷血症并在需要时按照剂量调整的指导方针[见剂量和给药2.2,2.3 ]。
5.3胚胎-胎儿毒性
根据动物繁殖研究的作用机理和研究结果,BALVERSA对孕妇服用可引起胎儿伤害。在一项胚胎胎儿毒性研究中,在器官发生期间口服erdafitinib对怀孕大鼠口服,导致母体暴露时的畸形和胚胎胎儿死亡低于基于曲线下面积的最大人类推荐剂量下的人类暴露( AUC)。建议孕妇注意胎儿的潜在危险。建议有生育潜力的女性患者在BALVERSA治疗期间以及最后一次用药后的一个月内使用有效的避孕方法。建议具有生殖潜能的女性伴侣的男性患者在BALVERSA治疗期间以及最后一次给药后的一个月内使用有效的避孕方法[请参阅使用在特殊人群(8.1,8.3)和临床药理学(12.1) ]。
6不良反应
标签中其他地方还描述了以下严重不良反应:
· 眼部疾病[请参阅警告和注意事项(5.1) ]。
· 高磷酸盐血症[见警告和注意事项(5.2) ]。
6.1临床试验经验
由于临床试验是在广泛不同的条件下进行的,因此不能将在某种药物的临床试验中观察到的不良反应率直接与另一种药物的临床试验中观察到的不良反应率进行比较,并且可能无法反映实际中观察到的不良反应率。
BAL2001的研究评估了BALVERSA的安全性,该研究包括87例局部晚期或转移性尿路上皮癌患者,这些患者患有敏感的FGFR3或FGFR2基因改变,并且在至少一线既往化疗期间或之后进展,包括新辅助治疗或新辅助治疗后12个月内辅助化疗[见临床研究(14.1) ]。每天一次口服8 mg BALVERSA治疗患者;在第1个周期的第14天,磷酸盐水平<5.5 mg / dL的患者剂量增加到9 mg,中位治疗时间为5.3个月(范围:0至17个月)。
最常见的不良反应(ARs)包括实验室异常(≥20%)为磷酸盐增加,口腔炎,疲劳,肌酐增加,腹泻,口干,强直分解,丙氨酸氨基转移酶增加,碱性磷酸酶增加,钠减少,食欲下降,白蛋白减少,味觉障碍,血红蛋白减少,皮肤干燥,天冬氨酸转氨酶增加,镁减少,干眼症,脱发,手掌plant足红斑综合症,便秘,磷酸盐减少,腹痛,钙增加,恶心和肌肉骨骼疼痛。最常见的3级或3级以上AR(> 1%)是口腔炎,指甲营养不良,掌plant红斑感觉异常综合征,甲沟炎,指甲疾病,角膜炎,强直溶解和高磷血症。
在1%的患者中,具有致命后果的不良反应是急性心肌梗塞。
41%的患者发生了严重的不良反应,包括眼部疾病(10%)。
13%的患者因不良反应而永久停药。永久性停药的最常见原因包括眼部疾病(6%)。
68%的患者出现剂量中断。需要停药的最常见不良反应包括高磷酸盐血症(24%),口腔炎(17%),眼部疾病(17%)和掌-红斑性感觉异常综合征(8%)。
53%的患者剂量减少。降低剂量最常见的不良反应包括眼部疾病(23%),口腔炎(15%),高磷酸盐血症(7%),掌-红斑性感觉异常综合征(7%),甲沟炎(7%)和指甲营养不良( 6%)。
表3列出了在每天一次8mg的BALVERSA治疗的≥10%的患者中报告的AR。
| 表3:≥10%(任何级)或≥5%(3-4级)患者的不良反应报告 | ||
| BALVERSA每天8毫克(N = 87) | ||
| 不良反应 | 所有级(%) | 3-4级(%) |
| 任何 | 100 | 67 |
| 胃肠道疾病 | 92 | 24 |
| 口腔炎 | 56 | 9 |
| 腹泻 | 47 | 2 |
| 口干 | 45 | 0 |
| 便秘 | 28 | 1 |
| 腹部疼痛* | 23 | 2 |
| 恶心 | 21 | 1 |
| 呕吐 | 13 | 2 |
| 代谢与营养失调 | 90 | 16 |
| 食欲下降 | 38 | 0 |
| 一般疾病和管理。现场条件 | 69 | 13 |
| 疲劳† | 54 | 10 |
| 发热 | 14 | 1 |
| 皮肤和皮下疾病 | 75 | 16 |
| 甲解‡ | 41 | 10 |
| 干性皮肤§ | 34 | 0 |
| 掌-红斑麻醉 | 26 | 6 |
| 脱发症 | 26 | 0 |
| 指甲变色 | 11 | 0 |
| 眼疾 | 62 | 11 |
| 干眼症¶ | 28 | 6 |
| 视力模糊 | 17 | 0 |
| 流泪增加 | 10 | 0 |
| 神经系统疾病 | 57 | 5 |
| 味觉障碍 | 37 | 1 |
| 感染和侵扰 | 56 | 20 |
| 甲沟炎 | 17 | 3 |
| 尿路感染 | 17 | 6 |
| 结膜炎 | 11 | 0 |
| 呼吸,胸和纵隔疾病 | 40 | 7 |
| 口咽痛 | 11 | 1 |
| 呼吸困难# | 10 | 2 |
| 肾和尿路疾病 | 38 | 10 |
| 血尿 | 11 | 2 |
| 肌肉骨骼和结缔组织疾病 | 31 | 0 |
| 肌肉骨骼疼痛Þ | 20 | 0 |
| 关节痛 | 11 | 0 |
| 调查 | 44 | 5 |
| 重量减少ß | 16 | 0 |
*包括腹痛,腹部不适,上腹痛和下腹痛
†包括乏力,疲劳,嗜睡和不适
‡包括:强直性,强直性,指甲病,指甲营养不良和指甲皱纹
§包括皮肤干燥和口干症
¶包括干眼症,干眼症,角膜炎,异物感和角膜糜烂
#包括呼吸困难和劳累性呼吸困难
Þ包括背部疼痛,肌肉骨骼不适,肌肉骨骼疼痛,肌肉骨骼胸部疼痛,颈部疼痛,四肢疼痛
ß包括体重减轻和恶病质
| 表4:报告≥10%(所有级)或≥5%(3-4级)患者的实验室异常 | ||
| BALVERSA每天8毫克(N = 86 *) | ||
| 实验室异常 | 所有级(%) | 3-4级(%) |
| 血液学 | ||
| 血红蛋白减少 | 35 | 3 |
| 血小板减少 | 19 | 1 |
| 白细胞减少 | 17 | 0 |
| 中性粒细胞减少 | 10 | 2 |
| 化学 | ||
| 磷酸盐增加 | 76 | 1 |
| 肌酐增加 | 52 | 5 |
| 钠减少 | 40 | 16 |
| 丙氨酸转氨酶增加 | 41 | 1 |
| 碱性磷酸酶升高 | 41 | 1 |
| 白蛋白下降 | 37 | 0 |
| 天冬氨酸转氨酶增加 | 30 | 0 |
| 镁减少 | 30 | 1 |
| 磷酸盐减少 | 24 | 9 |
| 钙增加 | 22 | 3 |
| 钾增加 | 16 | 0 |
| 空腹血糖升高 | 10 | 0 |
*87名患者中的1名没有进行实验室检查。
7药物相互作用
7.1其他药物对BALVERSA的影响
表5总结了影响BALVERSA暴露或血清磷酸盐水平的药物相互作用及其临床管理。
| 表5:影响BALVERSA的药物相互作用 | |
|---|---|
| 中度CYP2C9或强CYP3A4抑制剂 | |
| 临床影响 | · BALVERSA与中度CYP2C9或强效CYP3A4抑制剂的共同给药增加erdafitinib的血浆浓度[见临床药理学(12.3) ]。 · erdafitinib血浆浓度升高可能导致与药物相关的毒性升高[见警告和注意事项(5) ]。 |
| 临床管理 | · 考虑用BALVERSA治疗期间不是中度CYP2C9或强CYP3A4抑制剂的替代疗法。 · 如果不可避免地要同时使用中度CYP2C9或强效CYP3A4抑制剂,应密切监测不良反应并考虑相应地调整剂量[见剂量和给药方法(2.3) ]。如果中度CYP2C9或强效CYP3A4抑制剂停药,在没有药物相关毒性的情况下,可增加BALVERSA剂量。 |
| 强CYP2C9或CYP3A4诱导剂 | |
| 临床影响 | · BALVERSA与CYP2C9或CYP3A4的强诱导剂并用可能会显着降低erdafitinib的血浆浓度[见临床药理学(12.3) ]。 · erdafitinib血浆浓度降低可能导致活性降低。 |
| 临床管理 | · 避免将CYP2C9或CYP3A4的强诱导剂与BALVERSA并用。 |
| 中度CYP2C9或CYP3A4诱导剂 | |
| 临床影响 | · 将BALVERSA与CYP2C9或CYP3A4的中度诱导剂共同给药可能会降低erdafitinib的血浆浓度[见临床药理学(12.3) ]。 · erdafitinib血浆浓度降低可能导致活性降低。 |
| 临床管理 | · 如果在BALVERSA治疗开始时必须同时给予中度CYP2C9或CYP3A4诱导剂,则按推荐剂量给予BALVERSA(根据第14至21天的血清磷酸盐水平,每天一次8 mg,有可能增加到每天9 mg一次) )。 · 如果根据血清磷酸盐水平和耐受性,在初始剂量增加期后必须共同给予中度CYP2C9或CYP3A4诱导剂,则将BALVERSA剂量增加至9 mg。 · 当CYP2C9或CYP3A4的中度诱导剂被终止时,以相同剂量继续BALVERSA,而没有药物相关的毒性反应。 |
| 血清磷酸盐水平改变剂 | |
| 临床影响 | · BALVERSA与其他血清磷酸盐水平改变剂的共同给药可能增加或降低血清磷酸盐水平[见药效学(12.2) ] · 由于血清磷酸盐水平改变剂(而不是厄达非替尼)引起的血清磷酸盐水平变化可能会干扰确定初始剂量(根据血清磷酸盐水平增加)所需的血清磷酸盐水平[见剂量和给药方法(2.3) ]。 |
| 临床管理 | · 根据血清磷酸盐水平(第14至21天),在开始剂量增加之前,应避免将血清磷酸盐水平改变剂与BALVERSA并用[见剂量和给药方法(2.3) ]。 |
7.2 BALVERSA对其他药物的作用
表6总结了BALVERSA对其他药物的影响及其临床管理。
| 表6:影响其他药物的BALVERSA药物相互作用 | |
|---|---|
| CYP3A4底物 | |
| 临床影响 | · BALVERSA与CYP3A4底物的共同给药可能会改变CYP3A4底物的血浆浓度[见临床药理学(12.3) ]。 · CYP3A4底物的血浆浓度改变可能导致CYP3A4底物的活性降低或毒性增加。 |
| 临床管理 | · 避免将BALVERSA与具有狭窄治疗指数的CYP3A4敏感底物并用。 |
| OCT2底物 | |
| 临床影响 | · BALVERSA与OCT2底物的共同给药可能会增加OCT2底物的血浆浓度[见临床药理学(12.3) ]。 · OCT2底物的血浆浓度升高可能会导致OCT2底物的毒性增加。 |
| 临床管理 | · 考虑不是OCT2底物的替代疗法,或考虑基于耐受性降低OCT2底物(例如二甲双胍)的剂量。 |
| P-糖蛋白(P-gp)底物 | |
| 临床影响 | · BALVERSA与P-gp底物的共同给药可能会增加P-gp底物的血浆浓度[见临床药理学(12.3) ]。 · P-gp底物的血浆浓度增加可能导致P-gp底物的毒性增加。 |
| 临床管理 | · 如果BALVERSA与P-gp底物的共同给药是不可避免的,则在给药具有较窄治疗指数的P-gp底物之前或之后至少6小时应分开进行BALVERSA给药。 |
8在特定人群中的使用
8.1怀孕
风险摘要
根据动物繁殖研究的作用机理和发现,当将BALVERSA施用给孕妇时,可能会造成胎儿伤害[见临床药理学(12.1) ]。目前尚无有关孕妇使用BALVERSA来告知与药物相关风险的数据。在器官发生过程中对怀孕的大鼠口服给予erdafitinib会导致母体暴露时的畸形和胚胎胎儿死亡,低于基于AUC的最大推荐人剂量下的人暴露(参见数据)。建议孕妇和女性生殖潜力对胎儿的潜在危险。
对于指定人群,估计的主要先天缺陷和流产的背景风险尚不清楚。所有怀孕都有出生缺陷,流产或其他不良后果的背景风险。在美国普通人群中,临床公认的怀孕中主要出生缺陷和流产的估计背景风险分别为2–4%和15–20%。
数据
动物资料
在一项胚胎胎儿毒性研究中,厄达菲替尼是在器官发生期间口服给怀孕的大鼠服用的。剂量≥4mg/ kg /天(根据AUC的最大推荐人剂量,孕产妇总暴露量<人类总暴露量的0.1%)会导致胚胎胎儿死亡,主要血管畸形和其他血管异常,肢体畸形(直肠,无)或畸形的长骨),增加了多条骨骼(椎骨,胸骨,肋骨)骨骼异常的发生率,并降低了胎儿体重。
8.2哺乳
风险摘要
没有关于人乳中存在erdafitinib或erdafitinib对母乳喂养的孩子或产奶量的影响的数据。由于母乳喂养的儿童可能会出现erdafitinib引起严重的不良反应,因此建议哺乳期妇女在BALVERSA治疗期间以及末次剂量后的一个月内不要母乳喂养。
8.3生殖潜力的男性和女性
验孕
建议在开始使用BALVERSA治疗之前,对具有生殖能力的女性进行妊娠试验。
避孕
女性
孕妇服用BALVERSA可能对胎儿造成伤害。劝告有生殖潜力的女性在BALVERSA治疗期间以及最后一次给药后的一个月内使用有效的避孕药[见在特定人群中使用(8.1) ]。
雄性
建议具有生殖潜能的女性伴侣的男性患者在BALVERSA治疗期间以及最后一次给药后的一个月内使用有效的避孕药[见在特定人群中使用(8.1) ]。
不孕症
女性
根据动物研究的结果,BALVERSA可能会损害具有生殖潜能的雌性的生育力[见非临床毒理学(13.1) ]。
8.4小儿使用
尚未确定BALVERSA在儿科患者中的安全性和有效性。
在对大鼠和狗进行的4周和13周重复剂量毒理学研究中,在最大推荐人剂量下的暴露量小于人暴露量(AUC)时,观察到的骨骼和牙齿中的毒性。在这两个物种的多条骨骼中均报告了软骨样发育不良/间皮增生,牙齿异常包括大鼠和狗的异常/不规则凹陷以及大鼠成牙本质细胞的变色和变性。
8.5老年用途
临床研究中的416名接受BALVERSA治疗的患者中,有65%年龄在65岁以上,有12%在75岁以上。在这些患者和年轻患者之间未观察到安全性或有效性的总体差异[见临床研究(14) ]。
8.6 CYP2C9弱代谢者
CYP2C9 * 3 / * 3基因型:CYP2C9 * 3 /* 3基因型患者的Erdafitinib血浆浓度预计更高。监测已知或怀疑具有CYP2C9 * 3 / * 3基因型的患者中不良反应的增加[参见Pharmacogenomics(12.5) ]。
11说明
Erdafitinib是BALVERSA中的活性成分,是一种激酶抑制剂。化学名称为N-(3,5-二甲氧基苯基)-N'-(1-甲基乙基)-N- [3-(1-甲基-1H-吡唑-4-基)喹喔啉-6-基]乙烷-1 ,2-二胺。厄达菲替尼为黄色粉末。在很宽的pH值范围内,它几乎不溶于或不溶于水,可自由溶于有机溶剂,几乎不溶于或几乎不溶于水,或不溶于水介质。分子式为C 25 H 30 N 6 O 2,分子量为446.56。
厄达菲替尼的化学结构如下
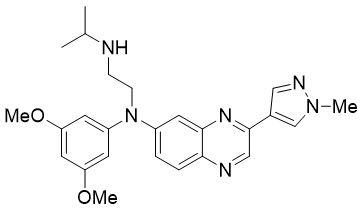
BALVERSA ®(erdafitinib)片剂被作为3毫克,4毫克或用于口服给药5mg的薄膜包衣片剂和包含下列非活性成分:
片剂核心:交联羧甲基纤维素钠,硬脂酸镁(来自植物来源),甘露醇,葡甲胺和微晶纤维素。
薄膜包衣:(欧巴代Amb II):一类甘油单辛酸癸酸酯,部分水解的聚乙烯醇,十二烷基硫酸钠,滑石粉,二氧化钛,氧化铁黄,氧化铁红(仅用于橙色和棕色片剂),二氧化三铁/铁氧化物黑(仅适用于棕色药片)。
12临床药理学
12.1行动机制
Erdafitinib是一种激酶抑制剂,可根据体外数据与FGFR1,FGFR2,FGFR3和FGFR4结合并抑制其酶促活性。Erdafitinib还与RET,CSF1R,PDGFRA,PDGFRB,FLT4,KIT和VEGFR2结合。Erdafitinib抑制FGFR磷酸化和信号传导,并降低表达FGFR遗传改变(包括点突变,扩增和融合)的细胞系中的细胞活力。Erdafitinib在表达FGFR的细胞系和源自包括膀胱癌在内的肿瘤类型的异种移植模型中显示出抗肿瘤活性。
12.2药效学
心脏电生理学
根据对187名癌症患者进行的开放标签,剂量递增和剂量扩展研究中QTc间隔的评估,厄达菲替尼对QTc间隔没有太大影响(即> 20 ms)。
血清磷酸盐
Erdafitinib由于FGFR抑制而增加了血清磷酸盐水平。BALVERSA应增加至最大推荐剂量,以在每日连续连续每日给药的早期周期中达到5.5-7.0 mg / dL的目标血清磷酸盐水平[参见剂量和用法(2.3) ]。
在erdafitinib临床试验中,除非没有替代品,否则禁止使用会增加血清磷酸盐水平的药物,例如磷酸钾补充剂,维生素D补充剂,抗酸剂,含磷酸盐的灌肠剂或缓泻剂,以及被禁止以磷酸盐为辅料的药物。 。为了控制磷酸盐的升高,允许使用磷酸盐粘合剂。避免与可能会在初始剂量增加之前根据血清磷酸盐水平改变血清磷酸盐水平的药物同时使用[见药物相互作用(7.1) ]。
12.3药代动力学
每天给药8 mg后,埃达菲替尼稳态最大观察血浆浓度(C max),曲线下面积(AUC tau)和最小观察血浆浓度(C min)的平均值(变异系数[CV%] )分别为1,399 ng / mL(51%),29,268 ng∙h / mL(60%)和936 ng / mL(65%)。
每天单次和重复一次给药后,在0.5至12 mg的剂量范围内,erdafitinib的暴露量(最大观察到的血浆浓度[C max ]和血浆浓度时间曲线下的面积[AUC])成比例增加。建议剂量)。每天给药2周后达到稳定状态,平均累积率为4倍。
吸收性
达到峰值血浆浓度(t max)的中位时间为2.5小时(范围:2至6小时)。
食物的作用
在健康受试者中服用高脂高热量餐(800卡路里至1,000卡路里,约占膳食总热量的50%)后,未观察到与erdafitinib药代动力学的临床意义差异。
分配
患者中厄达菲替尼的平均表观分布量为29L。
患者中的厄达菲替尼蛋白结合率为99.8%,主要与α-1酸性糖蛋白结合。
消除
患者的厄达菲替尼平均总表观清除率(CL / F)为0.362 L / h。
患者的厄达菲替尼平均有效半衰期为59小时。
代谢
Erdafitinib主要经CYP2C9和CYP3A4代谢。CYP2C9和CYP3A4在erdafitinib总清除率中的贡献分别估计为39%和20%。不变的erdafitinib是血浆中主要的药物相关部分,没有循环代谢物。
排泄
单次口服放射性标记的erdafitinib后,大约69%的剂量在粪便中恢复(未改变时为19%),在尿液中恢复到19%(未改变时为13%)。
特定人群
根据年龄(21–88岁),性别,种族,体重(36–132千克),轻度(eGFR [估计的肾小球滤过率,使用饮食调整的肾脏疾病],未观察到erdafitinib药代动力学的临床意义上的趋势。方程] 60至89 mL / min / 1.73 m 2)或中度(eGFR 30–59 mL / min /1.73 m 2)肾功能不全或轻度肝功能不全(总胆红素≤ULN和AST> ULN,或总胆红素> 1.0– 1.5×ULN和任何AST)。
erdafitinib在严重肾功能不全,需要透析的肾功能不全,中度或重度肝功能不全患者中的药代动力学尚不清楚。
药物相互作用研究
临床研究和基于模型的方法中度CYP2C9抑制剂:
Erdafitinib平均比率(90%CI)对C 最大和AUC INF分别为121%(99.9%,147)和148%(120,182),分别共同施用时与氟康唑,适度CYP2C9和CYP3A4抑制剂,相对于erdafitinib单独。
强CYP3A4抑制剂:
与伊曲康唑(一种强效CYP3A4抑制剂和P-gp抑制剂)共同给药时,C max和AUC inf的 Erdafitinib平均比率(90%CI)分别为105%(86.7,127)和134%(109,164)。相对于单独的erdafitinib。
强CYP3A4 / 2C9诱导剂:
模拟表明利福平(一种强CYP3A4/ 2C9诱导剂)可能显着降低erdafitinibC max和AUC。
体外研究
CYP底物:
Erdafitinib是CYP3A4的时间依赖性抑制剂和诱导剂。erdafitinib对敏感的CYP3A4底物的作用尚不清楚。Erdafitinib在临床相关浓度下不是其他主要CYP同工酶的抑制剂。
运输者:
Erdafitinib是P-gp的底物和抑制剂。预计P-gp抑制剂不会在临床上相关程度影响erdafitinib的暴露。Erdafitinib是OCT2的抑制剂。
Erdafitinib在临床相关浓度下不抑制BCRP,OATP1B,OATP1B3,OAT1,OAT3,OCT1,MATE-1或MATE-2K。
降酸剂:
Erdafitinib在1至7.4的pH范围内具有足够的溶解度。降酸剂(例如,抗酸剂,H 2拮抗剂,质子泵抑制剂)预计不会影响厄达菲替尼的生物利用度。
12.5药物基因组学
CYP2C9活性在具有遗传变异(例如CYP2C9 * 2和CYP2C9 * 3多态性)的个体中降低。CYP2C9 * 1 / * 2和* 1 / * 3基因型受试者的Erdafitinib暴露与CYP2C9 * 1 / * 1基因型受试者(野生型)相似。在以其他基因型(例如* 2 / * 2,* 2 / * 3,* 3 / * 3)为特征的受试者中没有可用数据。模拟表明在CYP2C9 * 2 / * 2和* 2 / * 3基因型的受试者中erdafitinib的暴露无临床意义的差异。预计在CYP2C9 * 3 / * 3基因型的受试者中erdafitinib的暴露量会增加50%,估计在各个族裔中的比例为0.4%至3%。
13毒理学
13.1致癌,诱变和生育能力受损
尚未与erdafitinib进行致癌性研究。
厄达菲替尼在细菌反向突变(Ames)分析中没有致突变性,在体外微核或体内大鼠骨髓微核分析中也不具有致胶性。
尚未使用厄达菲替尼进行动物生育力研究。在为期3个月的重复剂量毒性研究中,erdafitinib在最大推荐人剂量下的暴露量少于人暴露量(AUC),对大鼠雌性生殖器官(卵巢黄体坏死)产生了影响。
14临床研究
14.1具有易感FGFR基因改变的尿道上皮癌
BLC2001研究(NCT02365597)是一项多中心,开放标签,单组研究,旨在评估BALVERSA在局部晚期或转移性尿路上皮癌(mUC)患者中的疗效和安全性。通过临床试验测定法(CTA)确定用于筛选和招募患者的成纤维细胞生长因子受体(FGFR)突变状态。功效人群由参加本研究的87例患者组成,该患者在至少一种既往化疗中或之后进展,并且具有以下至少一种遗传变异:FGFR3基因突变(R248C,S249C ,G370C,Y373C)或FGFR基因融合体(FGFR3-TACC3,FGFR3-BAIAP2L1,FGFR2-BICC1,FGFR2-CASP7),由中央实验室进行的CTA确定。QIAGEN回顾性检查了69名患者的肿瘤样本therascreen ® FGFR RGQ RT-PCR试剂盒,这是FDA批准用于治疗患有MUC为BALVERSA选拔考试。
患者血清磷酸盐水平在第14天至第17天之间低于目标5.5 mg / dL的患者,每天接受一次8毫克BALVERSA的起始剂量,然后增加至每天9 mg的剂量。41%的患者出现剂量增加。给予BALVERSA直至疾病进展或出现不可接受的毒性。根据RECIST v1.1,由盲人独立审查委员会(BIRC)确定的主要疗效结果指标是客观缓解率(ORR)和缓解持续时间(DoR)。
中位年龄为67岁(范围:36至87岁),男性为79%,白人为74%。大多数患者(92%)的基线东部合作肿瘤小组(ECOG)表现状态为0或1。66%的患者发生内脏转移。八十四(97%)位患者先前曾接受过顺铂或卡铂中的至少一种。56%的患者仅接受先前的基于顺铂的治疗方案,29%的患者仅接受先前的基于碳铂的治疗方案,10%的患者接受了顺铂和基于卡铂的治疗方案。三名(3%)患者仅在先前接受含铂新辅助治疗或辅助治疗后才有疾病进展。24%的患者已接受过先前的抗PD-L1 / PD-1治疗。
疗效结果总结在表7和表8中。总的应答率为32.2%。响应者包括以前对PD-L1 / PD-1治疗无反应的患者。
| 表7:疗效结果 | |
| BIRC *评估 | |
| 终点 | N = 87 |
| ORR(95%CI) | 32.2%(22.4,42.0) |
| 完全反应(CR) | 2.3% |
| 部分反应(PR) | 29.9% |
| 数月的平均DoR(95%CI) | 5.4(4.2,6.9) |
ORR = CR + PR
CI =置信区间
*BIRC:盲人独立审查委员会
| 表8:FGFR基因改变的疗效结果 | |
| BIRC *评估 | |
| FGFR3点突变 | N = 64 |
| ORR(95%CI) | 40.6%(28.6,52.7) |
| FGFR3融合† ,‡ | N = 18 |
| ORR(95%CI) | 11.1%(0,25.6) |
| FGFR2融合‡ | N = 6 |
| ORR | 0 |
CI =置信区间
*BIRC:盲人独立审查委员会
†两位应答者均具有FGFR3-TACC3_V1融合
‡上面报道了FGFR2融合和FGFR3融合均报道了一名FGFR2-CASP7/ FGFR3-TACC3_V3融合患者
16供应/存储和处理方式
BALVERSA ®(erdafitinib)片剂下列优势和封装:
· 3 mg片:黄色,圆形双凸,薄膜包衣,在一侧凹陷有“ 3”,在另一侧凹陷了“ EF”。
–
一瓶56片带有儿童密封盖的药片(NDC 59676-030-56)。
–
带有儿童安全盖的84片瓶(NDC 59676-030-84)。
· 4 mg片剂:橙色,圆形双凸,薄膜包衣,在一侧凹有“ 4”,在另一侧凹有“ EF”。
–
带有儿童安全密封盖的28片瓶(NDC 59676-040-28)。
–
带有儿童安全密封盖的56片瓶(NDC 59676-040-56)。
· 5 mg片剂:褐色,圆形双凸,薄膜包衣,在一侧凹陷有“ 5”,在另一侧凹陷了“ EF”。
–
一瓶28片带有儿童密封盖的瓶子(NDC 59676-050-28)。
储存在20°C–25°C(68°F–77°F);允许在15°C和30°C(59°F和86°F)之间进行偏移[请参阅USP控制的室温]。
17患者咨询信息
建议患者阅读FDA批准的患者标签(患者信息)。
FGFR基因改变:建议患者在肿瘤标本中必须有易感FGFR3或FGFR2突变或基因融合的证据,以鉴定需要治疗的患者[见剂量和给药方法(2.1) ]。
眼部疾病:如果患者出现任何视觉变化,建议他们联系其医疗保健提供者[请参阅警告和注意事项(5.1) ]。为了预防或治疗干眼症,建议患者在清醒时间内至少每2小时频繁使用人工泪液替代品,为眼部凝胶或软膏保湿或润滑[见剂量和用法(2.3) ]。
皮肤,粘液或指甲疾病:如果患者出现进行性或无法忍受的皮肤,粘液或指甲疾病,建议患者联系其医疗保健提供者[见不良反应(6.1) ]。
高磷酸盐血症:建议患者其医疗保健提供者应在开始治疗的14到21天之间评估其血清磷酸盐水平,并在需要时调整剂量[见警告和注意事项(5.2) ]。在最初的磷酸盐评估期间,建议患者避免与可能改变血清磷酸盐水平的药物同时使用。告知患者,在最初的磷酸盐评估期之后,应在BALVERSA治疗期间每月对磷酸盐水平进行高磷血症监测[参见药物相互作用(7.1) ]。
药物相互作用:建议患者告知他们的医疗保健提供商都伴随药物,包括处方药,过度的非处方药和草药产品[见药物相互作用(7.1,7.2) ]。
剂量说明:指导患者每天带或不带食物全部吞服一次片剂。如果在服用BALVERSA之后的任何时间出现呕吐,建议患者第二天服用下一剂。[参见剂量和给药(2.1) ]。
错过剂量:如果错过剂量,建议患者尽快服用。第二天恢复BALVERSA的常规每日剂量表。不应服用额外的药片来弥补错过的剂量[见剂量和用法(2.3) ]。
胚胎-胎儿毒性:建议孕妇和具有潜在胎儿生殖危险的女性。劝告女性告知其已知或怀疑怀孕的医疗人员[请参阅警告和注意事项(5.3)和特定人群的使用(8.1) ]。建议有生育潜力的女性患者在治疗期间以及最后一次服用BALVERSA后一个月内使用有效的避孕方法。建议具有生殖潜能的女性伴侣的男性患者在治疗期间以及最后一次服用BALVERSA后一个月内使用有效的避孕药[见在特定人群中使用(8.3) ]。
哺乳期:建议女性在BALVERSA治疗期间和最后一次服药后一个月内不要母乳喂养[见在特定人群中使用(8.2) ]。
| 患者信息 BALVERSA ®(BAL-VER-SAH) (erdafitinib)片剂 | |
|---|---|
| 什么是BALVERSA? BALVERSA是一种处方药,用于治疗已扩散或无法通过手术切除的膀胱癌(尿路上皮癌)成人: · 具有某种类型的异常“ FGFR”基因,并且 · 他们曾经尝试过至少一种其他含铂的化学治疗药物,但这种药物无效或不再起作用。 您的医疗保健提供者将测试您的癌症是否存在某些类型的异常FGFR基因,并确保BALVERSA适合您。 尚不知道BALVERSA在儿童中是否安全有效。 | |
| 服用BALVERSA之前,请告知您的医疗保健提供者您的所有医疗状况,包括是否: · 有视力或眼睛问题。 · 正在怀孕或打算怀孕。BALVERSA可能会伤害未出生的婴儿。使用BALVERSA治疗期间,您不应怀孕。 可以怀孕的女性: o 您的医疗保健提供者可能会在您开始使用BALVERSA治疗之前进行妊娠试验。 o 在治疗期间和最后一次服用BALVERSA后1个月内,您应使用有效的节育措施。与您的医疗保健提供者讨论可能适合您的节育方法。 o 如果您怀孕或认为自己可能怀孕,请立即告诉您的医疗保健提供者。 男性和女性伴侣可以怀孕: o 在使用BALVERSA治疗期间以及在最后一次服药后1个月内进行性活动时,您应该使用有效的节育措施。 · 正在母乳喂养或计划母乳喂养。在治疗期间以及最后一次服用BALVERSA后1个月内请勿母乳喂养。 告诉您的医护人员您服用的所有药物,包括处方药和非处方药,维生素和草药补品。 | |
| 我应该如何服用BALVERSA? · 完全按照医疗保健提供者的指示服用BALVERSA。 · 每天服用BALVERSA 1次。 · 吞食BALVERSA整片含或不含食物。 · 您的医疗保健提供者可能会改变您的BALVERSA剂量,如果您出现某些副作用,则暂时停止或完全停止治疗。 · 如果您错过了BALVERSA的剂量,请尽快在同一天服用。第二天服用常规剂量的BALVERSA。BALVERSA的服用量不要超过处方,以弥补错过的剂量。 · 如果您服用BALVERSA后呕吐,请勿服用其他BALVERSA平板电脑。第二天服用常规剂量的BALVERSA。 | |
| BALVERSA可能有哪些副作用? BALVERSA可能引起严重的副作用,包括: · 眼睛问题。BALVERSA常见于眼睛问题,但也可能很严重。眼睛问题包括眼睛干涩或发炎,角膜发炎(眼睛的前部)和视网膜内部的视网膜疾病。如果您出现视力模糊,视力丧失或其他视觉变化,请立即告知您的医疗保健提供者。您应在清醒时间内至少每2小时使用人工泪液替代品,保湿或润滑眼部凝胶或软膏,以防止眼睛干涩。在使用BALVERSA进行治疗期间,您的医疗保健提供者将送您去看眼科医生。 · 血液中磷酸盐含量高(高磷酸盐血症)。高磷酸盐血症在BALVERSA中很常见,但也可能很严重。您的医疗保健提供者将在开始使用BALVERSA治疗之后的14到21天之间检查您的血液磷酸盐水平,然后每月检查一次,如果需要,可以更改剂量。 BALVERSA最常见的副作用包括: | |
| · 口疮 · 感觉累了 · 肾功能改变 · 腹泻 · 口干 · 指甲与床分开或指甲形成不良 · 肝功能改变 · 盐(钠)含量低 · 食欲下降 · 味觉改变 | · 低血红细胞(贫血) · 皮肤干燥 · 眼睛干涩 · 脱发 · 主要在手或脚上发红,肿胀,脱皮或压痛(“手足综合症”) · 便秘 · 胃(腹部)疼痛 · 恶心 · 肌肉疼痛 |
| 如果您出现任何指甲或皮肤问题,请立即告诉您的医疗服务提供者,包括指甲从指甲床分离,指甲疼痛,指甲出血,指甲断裂,指甲颜色或质地改变,指甲周围的皮肤受到感染,皮肤发痒等皮疹,皮肤干燥或皮肤裂缝。 BALVERSA可能会影响能够怀孕的女性的生育能力。如果您担心此问题,请与您的医疗保健提供者联系。 这些并非BALVERSA的所有可能的副作用。有关更多信息,请咨询您的医疗保健提供者或药剂师。 致电您的医疗保健提供者以获取有关副作用的医疗建议。您可以通过1-800-FDA-1088向FDA报告副作用。 | |
| 我应该如何储存BALVERSA? · 将BALVERSA片剂存放在68°F至77°F(20°C至25°C)的室温下。 将BALVERSA和所有药物放在儿童接触不到的地方。 | |
| 有关安全有效使用BALVERSA的一般信息。 除患者信息单张中列出的药物外,有时还会开出其他药物。请勿在没有规定的条件下使用BALVERSA。即使他人有与您相同的症状,也不要将BALVERSA给予他人。可能会伤害他们。如果您需要更多信息,请与您的医疗保健提供者联系。您可以向您的医疗保健提供者询问为医疗保健专业人员编写的有关BALVERSA的信息。 | |
| BALVERSA中的成分是什么? 活性成分: erdafitinib 无效成分: 片剂核心:交联羧甲基纤维素钠,硬脂酸镁(来自植物来源),甘露醇,葡甲胺和微晶纤维素。 薄膜包衣(欧巴代Amb II):I型单辛酸甘油酯,部分水解的聚乙烯醇,十二烷基硫酸钠,滑石粉,二氧化钛,氧化铁黄,氧化铁红(仅用于橙色和棕色片剂),二氧化三铁/氧化铁黑色(仅适用于棕色药片)。 | |

