处方资料重点
美国初步批准:2018 年
适应证和用途
适用于以下ALK阳性突变的转移性非小细胞肺癌治疗后进展:
(1)克唑替尼或者至少一种其他ALK抑制剂使用后;
(2)阿来替尼作为一线治疗后;
(3)塞瑞替尼作为一线治疗后。
剂量和给药方法
建议口服剂量为 100 毫克,每日一次(2.1)
剂型和规格
片剂:25 毫克或 100 毫克
禁忌证
与强CYP3A诱导剂同时使用
警告和注意事项
(1)伴随使用强CYP3A诱导剂的严重肝毒性风险:停用强CYP3A诱导剂治疗至少3个血浆半衰期后,再开始使用LORBRENA;(2.3,5.1)
(2)中枢神经系统(CNS)效应:中枢神经系统的影响包括癫痫发作,幻觉和认知功能的改变,情绪(包括自杀意念),言语,精神状态和睡眠。延缓给药或减量用药,或根据严重程度永久停止LORBRENA。(2.2,5.2)
(3)高脂血症:开始或增加降脂剂的剂量。根据严重程度,延迟或减量使用LORBRENA。(2.2,5.3)
(4)房室传导阻滞:根据严重程度,延迟或减量使用LORBRENA。(2.2,5.4)
(5)间质性肺病/肺炎:在怀疑患有间质性肺病/肺炎的患者应立即停用LORBRENA。并且应永久停药。(2.2,5.5)
(6)胚胎-胎儿毒性:可能导致胎儿伤害。告知女性对胎儿有潜在风险的生殖潜力。建议具有生殖潜力的男性和女性使用有效的非激素避孕方法。(5.6,7.2,8.1,8.3)
不良反应
常见的不良反应(≥20%)包括水肿,周围神经病,认知效应,呼吸困难,疲劳,体重增加,关节痛,情绪影响和腹泻。(6.1)
药物相互作用
Cyp3a诱导剂:禁用于强CYP3A 诱导剂。避免与中度CYP3A诱导剂同时使用。(2.3,7.1)
Cyp3a抑制剂:避免与强的CYP3A抑制剂同时使用; 如果不能避免同时使用,则减少 lobrena 剂量。 (2.4,7.1)
Cyp3a底物:避免与CYP3A底物同时使用,如果浓度变化很小可能导致严重的治疗失败。(7.2)
在特殊人群中使用
● 哺乳:建议妇女不要哺乳喂养。
完整处方资料
1 适应证和用途
Lobrena 用于治疗间变性淋巴瘤激酶阳性的转移性非小细胞肺癌(NSCLC) 克唑替尼和至少一种其他ALK 抑制剂治疗转移性疾病;或
Alectinib作为第一个转移性疾病的 ALK 抑制剂治疗;
ceritinib作为第一个转移性疾病的 ALK 抑制剂治疗。
基于肿瘤反应率和反应持续时间的加速审批批准这一适应症[参见临床研究(14.1)]。继续批准这一适应症可能 取决于验证和说明临床利益的确认试验。
2 剂量和给药方法
2.1 推荐剂量
Lobrena的推荐剂量为每日口服 100 毫克,不论是否进食,直至病情恶化或出现不可接受的毒性[见临床药理学(12.3)]。
整个吞下药片。不要咀嚼、压碎或分割药片。如果药片破碎、破裂或其他不完整,不要食用。
每天同一时间服用Lobrena。如果错过了一次剂量,除非下一次剂量在 4 小时内到期,否则服用错过的剂量。不要同时服用两剂以弥补错过的剂量。 如果 lobrena 后出现呕吐,请不要服用额外剂量,但要继续服用下一剂。
2.2 不良反应的剂量修改
建议减少的剂量如下:
第一剂量减量:lobrena75毫克,口服,每日一次
第二剂量减量:每日一次,每次口服50毫克
无法每天口服一次50 mg的患者,永久停用LORBRENA。
Lobrena不良反应的剂量修改见表 1。

2.3 同时使用强或中度 CYP3A 诱导剂
服用强效CYP3A诱导剂的患者禁用LORBRENA。 在开始LORBRENA之前,中断强效CYP3A诱导剂的3次血浆半衰期,直到强效CYP3A诱导剂。 避免将LORBRENA与中度CYP3A诱导剂同时使用[见警告和注意事项(5.1),临床药理学(12.3)]。
2.4强效CYP3A抑制剂的剂量修改
避免将LORBRENA与强效CYP3A抑制剂同时使用。如果不能避免与强效CYP3A抑制剂同时使用,则将LORBRENA的起始剂量从每天一次口服100 mg减至每天一次口服75 mg。
在因不良反应口服减低剂量至每天一次75 mg且开始使用强效CYP3A抑制剂的患者中,将LORBRENA剂量减低至口服一次每天50 mg。如果停止同时使用强效CYP3A抑制剂,请将LORBRENA剂量(在强效CYP3A抑制剂的3个血浆半衰期后)增加至开始使用强效抑制剂之前的剂量[见临床药理学(12.3)]。
3剂型和强度
片剂:
25 mg:8毫米圆形,棕褐色,立即释放,薄膜包衣,在一侧刻有“ Pfizer”,另一侧刻有“ 25”和“ LLN”
100 mg:8.5毫米×17毫米椭圆形,熏衣草,立即释放,薄膜包衣,一侧凹陷有“辉瑞(Pfizer)”,另一侧凹陷有“ LLN 100”
4禁忌症
服用强效CYP3A诱导剂的患者禁用LORBRENA,因为其可能具有严重的肝毒性[见警告和注意事项(5.1)]。
5警告和注意事项
5.1并用强效CYP3A诱导剂引起严重肝毒性的风险
接受单剂LORBRENA和每日多次利福平(一种强CYP3A诱导剂)的12位健康受试者中有10位发生严重肝毒性。 50%的受试者发生4级丙氨酸氨基转移酶(ALT)或天冬氨酸氨基转移酶(AST)升高,33%的患者发生3级ALT或AST升高,而8%发生2级ALT或AST升高。 ALT或AST升高在3天内发生,在中位数15天(7到34天)后恢复到正常范围内; ALT或AST升高为3或4级的受试者中位恢复时间为18天,ALT或AST升高为2级的患者中位恢复时间为7天。
服用强效CYP3A诱导剂的患者禁用LORBRENA。在开始LORBRENA之前,中断强效CYP3A诱导剂的3次血浆半衰期,直到强效CYP3A诱导剂。
避免将LORBRENA与中度CYP3A诱导剂同时使用。如果不能避免同时使用中度CYP3A诱导剂,则在开始LORBRENA的48小时后和开始LORBRENA的第一周内至少监测3次AST,ALT和胆红素。
根据每种药物的相对重要性,中断LORBRENA或CYP3A诱导剂以持续存在2级或更高的肝毒性[见临床药理学(12.3)]。
5.2中枢神经系统效应
广泛的中枢神经系统(CNS)的影响可以发生在接受LORBRENA的病人。这些包括癫痫,幻觉,认知功能的改变,情绪(包括自杀的想法),语言,精神状态和睡眠。总的来说,接受LORBRENA治疗的患者中有54%出现中枢神经系统效应[参见不良反应(6.1)]。在B7461001研究中,332名接受任何剂量洛布伦娜治疗的患者中,29%的人有认知效果;这些事件中有2.1%是严重的(3级或4级)。1.8%的这些事件是严重的。14%的患者出现言语障碍;其中0.3%是严重的。7%的患者出现幻觉;其中0.6%是严重的。2.1%的患者出现精神状态改变;1.8%的这些事件是严重的。发作发生在3%的病人,有时与其他神经学发现。10%的患者有睡眠问题。首次出现中枢神经系统症状的平均时间为1.2个月(1天至1.7年)。总的来说,1.5%的患者需要永久性停用洛布伦纳以达到中枢神经系统的效果;9%需要临时停药,8%需要减少剂量。
根据LORBRENA的严重程度,保留并恢复相同剂量或减少剂量或永久停用洛布伦娜[参见剂量和给药(2.2)]。
5.3高脂血症
接受LORBRENA治疗的患者可出现血清胆固醇和甘油三酯升高[参见不良反应(6.1)]。在B7461001研究中接受LORBRENA治疗的332名患者中,总胆固醇3级或4级升高17%,甘油三酯3级或4级升高17%。高胆固醇血症和高甘油三酯血症的中位发病时间均为15天。大约7%的患者需要暂时停药,3%的患者需要减少洛布雷纳的剂量,以提高胆固醇和甘油三酯。80%的患者需要开始服用降脂药物,从开始服用降脂药物的平均时间为21天。
在高脂血症患者中开始或增加降脂药物的剂量。监测血清胆固醇和甘油三酯开始前,1和2个月后,开始LORBRENA,然后定期。对第一次发病保留并恢复相同剂量;根据复发的严重程度恢复相同或减少洛布伦纳的剂量[参见剂量和给药(2.2)]。
5.4房室传导阻滞
接受LORBRENA治疗的患者可发生PR间隔延长和房室传导阻滞(AV)[不良反应(6.1),临床药理学(12.2)]。295例在B7461001研究中每日口服100毫克洛布伦纳的患者中,基线心电图(ECG)为1%的患者出现房室传导阻滞,0.3%的患者出现3级房室传导阻滞,并进行了起搏器放置。
在开始使用LORBRENA之前和之后定期监测心电图。保留和恢复在减少剂量或相同剂量的病人谁接受起搏器安置。无起搏器的患者因复发而永久停药[参见剂量和给药(2.2)]。
5.5间质性肺病/肺炎
严重的或危及生命的肺不良反应,与肺间质疾病(ILD)/肺炎可以发生与LORBRENA。在接受治疗的患者中,有1.5%发生了ILD/肺炎
在B7461001研究中的任何剂量的LORBRENA,包括1.2%的3级或4级ILD/肺炎。1例(0.3%)因ILD/肺炎停用洛布瑞娜。
如发现呼吸道症状恶化(如呼吸困难、咳嗽、发烧等),应立即调查是否有固体/肺炎。立即停止洛布伦纳在怀疑固体肺炎/肺炎患者。对于任何严重程度的与治疗相关的ILD/肺炎,永久性停用LORBRENA[参见剂量和用药(2.2)]。
5.6 胎儿毒性
根据动物研究的结果及其作用机理,当对孕妇服用时,LORBRENA可能引起胎儿伤害。在每天一次建议剂量为100mg的母体暴露下,通过口服管饲法对怀孕的大鼠和兔子进行lorlatinib的口服灌胃,会导致畸形,植入后损失增加和流产,而孕产妇的暴露量等于或小于人类暴露量基于曲线下的面积(AUC)。
建议孕妇注意胎儿的潜在危险。建议具有生殖潜力的女性使用有效的非激素避孕方法,因为在用LORBRENA治疗期间以及最终剂量后至少6个月内,LORBRENA可使激素避孕药无效。建议具有生殖潜力的女性伴侣在LORBRENA治疗期间和最终剂量后3个月内使用有效的避孕药[见药物相互作用(7.2),在特定人群中的使用(8.1、8.3),非临床毒理学(13.1)]。
6 不良反应
标签上其他地方描述了以下不良反应:
同时使用强效CYP3A诱导剂有严重肝毒性的危险[见警告和注意事项(5.1)]
中枢神经系统作用[请参阅警告和注意事项(5.2)]
高脂血症[请参阅警告和注意事项(5.3)]
房室传导阻滞[请参阅警告和注意事项(5.4)]
间质性肺疾病/肺炎[请参阅警告和注意事项(5.5)]
6.1临床试验经验
由于临床试验是在广泛不同的条件下进行的,因此不能将在某种药物的临床试验中观察到的不良反应率直接与另一种药物的临床试验中观察到的不良反应率进行比较,并且可能无法反映实际中观察到的不良反应率。
警告和注意事项中的数据反映了332例ALK阳性或ROS1阳性,转移性非小细胞肺癌(NSCLC)患者的LORBRENA暴露,该患者参加了多队列,多国,非对照,剂量寻找和活性评估试验(研究B7461001),他接受LORBRENA的剂量为单剂量或分剂量,每日剂量为10毫克至200毫克。
下述数据反映了在研究B7461001中,每天口服一次LORBRENA 100毫克的295名ALK阳性或ROS1阳性转移性NSCLC患者暴露于LORBRENA。暴露于LORBRENA的中位时间为12.5个月(1天至35个月),其中52%接受LORBRENA≥12个月。患者特征为中位年龄为53岁(19至85岁),年龄≥65岁(18%),女性(58%),白人(49%),亚洲人(37%)和东部合作肿瘤小组(ECOG) )效果状态0或1(96%)。
最常见的不良反应(≥20%)为水肿,周围神经病变,认知障碍,呼吸困难,疲劳,体重增加,关节痛,情绪障碍和腹泻。最常见(≥20%)的实验室异常是高胆固醇血症,高甘油三酯血症,贫血,高血糖症,AST升高,白蛋白血症,ALT升高,脂肪酶升高和碱性磷酸酶升高。
295例患者中有32%发生严重不良反应。最常见的严重不良反应是肺炎(3.4%),呼吸困难(2.7%),发热(2%),精神状态改变(1.4%)和呼吸衰竭(1.4%)。致命不良反应发生在2.7%的患者中,包括肺炎(0.7%),心肌梗塞(0.7%),急性肺水肿(0.3%),栓塞(0.3%),周围动脉闭塞(0.3%)和呼吸窘迫(0.3%)。 8%的患者永久终止了LORBRENA的不良反应。
导致永久停药的最常见不良反应是呼吸衰竭(1.4%),呼吸困难(0.7%),心肌梗塞(0.7%),认知影响(0.7%)和情绪影响(0.7%)。大约48%的患者需要中断剂量。导致剂量中断的最常见不良反应是水肿(7%),高甘油三酯血症(6%),周围神经病变(5%),认知作用(4.4%),脂肪酶升高(3.7%),高胆固醇血症(3.4%),情绪影响(3.1%),呼吸困难(2.7%),肺炎(2.7%)和高血压(2.0%)。大约24%的患者需要减少至少1剂不良反应剂量。导致剂量减少的最常见不良反应是水肿(6%),周围神经病变(4.7%),认知作用(4.1%)和情绪影响(3.1%)。
表2和3分别总结了在研究B7461001中接受LORBRENA治疗的患者的常见不良反应和实验室异常。
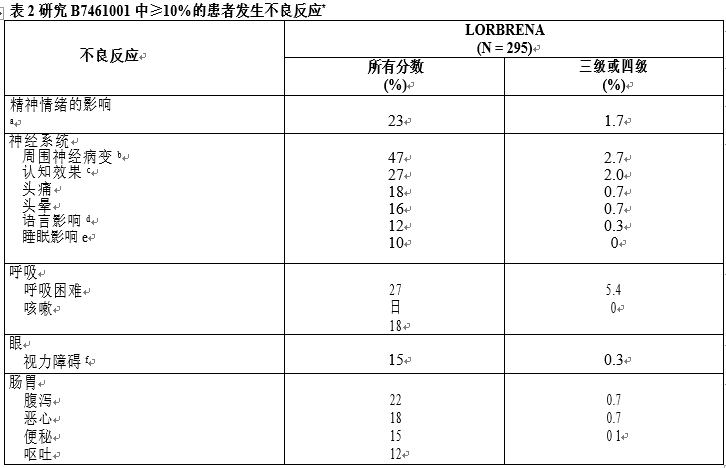
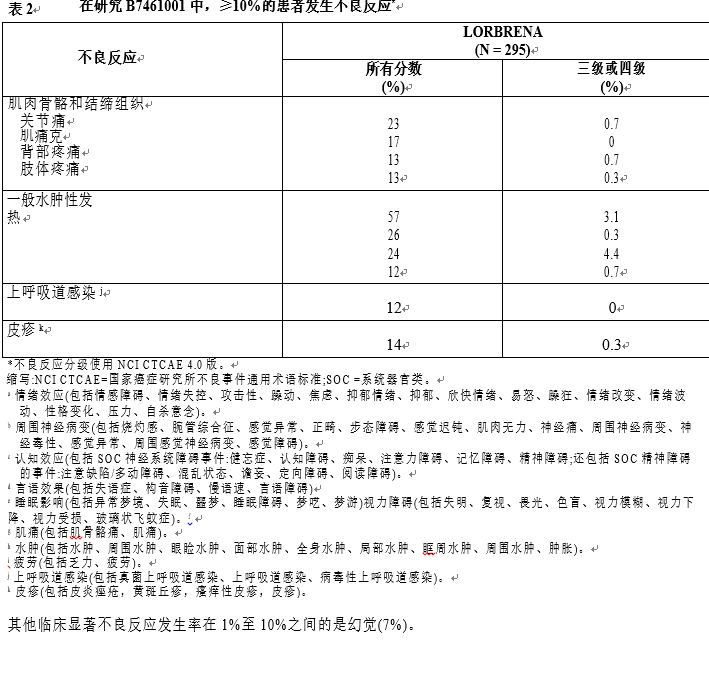
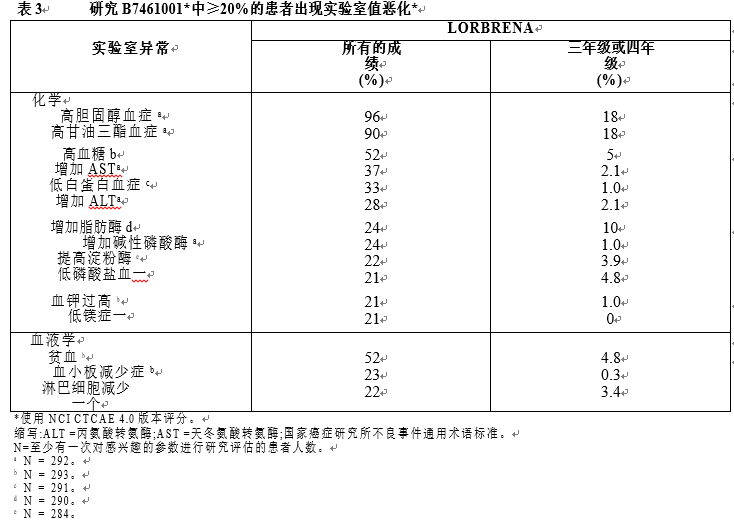
7药物的相互作用
7.1其他药物对LORBRENA的影响
CYP3A诱导剂的作用
与强CYP3A诱导剂同时使用LORBRENA降低了lorlatinib的血浆浓度,这可能会降低LORBRENA的疗效。目前还没有研究在适当的CYP3A诱导剂作用下同时使用LORBRENA对lorlatinib血浆浓度的影响。
接受利福平(一种强CYP3A诱导剂)治疗的健康受试者出现严重的肝毒性。在12名健康受试者中,接受单次100毫克洛布伦那和每日多次服用利福平的情况下,83%的受试者的ALT或AST出现3级或4级的升高,8%的受试者的ALT或AST出现2级的升高。肝毒性的一种可能机制是罗勃拉和利福平激活孕烷X受体(PXR),它们都是PXR激动剂。同时使用LORBRENA和中等剂量的CYP3A诱导剂(也是PXR激动剂),肝毒性的风险是未知的。
服用强CYP3A诱导剂的患者禁用LORBRENA。在启动LORBRENA之前,停用强CYP3A诱导剂,使用强CYP3A诱导剂的3个等离子半衰期。
避免与中度CYP3A诱导剂同时使用LORBRENA。如果不能避免同时使用中等剂量的CYP3A诱导剂,则按照建议监测ALT、AST和胆红素[参见剂量和给药(2.3)、警告和预防(5.1)、临床药理学(12.3)]。
强CYP3A抑制剂的作用
与强CYP3A抑制剂同时使用会增加洛雷替尼的血浆浓度,这可能会增加洛雷替尼不良反应的发生率和严重程度。避免同时使用LORBRENA与强CYP3A抑制剂。如果不能避免同时使用,则按照建议减少洛布伦纳的剂量[参见剂量和给药(2.4),临床药理学(12.3)]。
7.2 LORBRENA对其他药物的影响
CYP3A基质
同时使用LORBRENA会降低CYP3A底物的浓度[参见临床药理学(12.3)],这可能会降低这些底物的疗效。避免同时使用LORBRENA与CYP3A底物,其中最小的浓度变化可能导致严重的治疗失败。如果无法避免同时使用,则按照批准的产品标签增加CYP3A底物的用量。
8用于特定人群
8.1怀孕
风险概述
基于动物研究的结果及其作用机制[参见临床药理学(12.1)],洛布伦纳给孕妇服用时可造成胚胎-胎儿损害。目前还没有关于洛布伦纳在孕妇中使用的数据。管理lorlatinib怀孕期间口服填喂法大鼠和兔子的器官发生导致畸形,post-implantation损失增加,和堕胎在孕产妇曝光等于或小于人类接触的推荐剂量100毫克每天一次基于AUC(参见数据)。建议孕妇注意对胎儿的潜在危险。
在美国普通人群中,在临床诊断的怀孕中,重大出生缺陷和流产的背景风险估计分别为2- 4%和15 - 20%。
数据
动物的数据
在大鼠和家兔体内进行了初步的胚胎-胚胎发育研究,探讨了洛拉替尼在器官发生过程中的作用。在家兔中,洛拉替尼给药剂量为15mg/kg(约为建议剂量100 mg的3倍)或更大时,可导致流产和妊娠完全流产。当剂量为4 mg/kg时(约为人体推荐剂量100mg的0.6倍),毒性包括植入后增加的损失和畸形,包括旋转的肢体、畸形的肾脏、圆顶的头部、高拱形的上颚和脑室的扩张。在大鼠中,以4mg/kg剂量给药洛拉替尼可导致妊娠完全丧失(约为推荐剂量100 mg时人类接触剂量的5倍)或更高。当剂量为1mg/kg时(约等于人体在推荐剂量为100 mg时的暴露量),植入后损失增加,胎儿体重下降,畸形包括胃裂、旋转肢体、多余的手指和血管异常。
8.2哺乳
风险概述
目前还没有关于洛拉替尼或其代谢物存在于人类或动物的牛奶中,或其对母乳喂养婴儿或牛奶生产的影响的数据。由于母乳喂养的婴儿可能出现严重的不良反应,建议妇女在接受洛布雷纳治疗期间和最后一次给药后7天内不要母乳喂养。
8.3具有生殖潜能的女性和男性
怀孕测试
在开始使用LORBRENA之前,验证具有生育潜力的女性的怀孕状况[参见在特定人群中的使用(8.1)]。
避孕
当给孕妇使用LORBRENA时,会导致胚胎-胎儿损害[参见在特定人群中的使用(8.1)]。
女性
建议有生育潜力的女性患者在接受洛布伦娜治疗期间,以及在最后一次给药后至少6个月,使用有效的非激素避孕措施。建议有生育潜力的女性使用非激素避孕方法,因为洛布伦娜会使激素避孕无效[参见药物相互作用(7.2)]。
男性
基于基因毒性的发现,建议有生育潜力的男性和女性伴侣在使用洛布伦娜治疗期间以及最终剂量后至少3个月期间使用有效的避孕措施[参见非临床毒理学(13.1)]。
不孕不育
男性
根据动物研究的结果,LORBRENA可能会暂时损害男性生育能力[参见非临床毒理学(13.1)]。
8.4儿童使用
洛布伦纳用于儿童患者的安全性和有效性尚未确定。
8.5老年使用
在B7461001研究的295名患者中,18%的患者年龄在65岁或65岁以上。虽然数据有限,但在65岁或65岁以上的患者和65岁以下的患者之间,并没有观察到在安全性或有效性方面的临床重要差异。
8.6肝损伤
轻度肝损害患者(AST > ULN时总胆红素≤正常[ULN]上限,AST时总胆红素>1~ 1.5×ULN)不建议调整剂量。对于中度或重度肝功能损害患者,洛布伦纳的推荐剂量尚未确定[参见临床药理学(12.3)]。
8.7肾功能损害
轻度或中度肾功能损害患者不建议调整剂量(Cockcroft-Gault估计肌酐清除率[CLcr] 30 ~89 mL/min)。对于严重肾功能损害的患者,洛布伦纳的推荐剂量尚未确定[参见临床药理学(12.3)]。
11 描述
LORBRENA (lorlatinib)是一种口服激酶抑制剂。分子式为无水CHFNO,分子量为406.41道尔顿。211962其化学名称为(10R)-7-氨基-12-氟-2,10,16-三甲基-15-氧-10,15,16,17-四氢- 2h -4,8-甲基吡唑啉[4,3-h][2,5,11]
benzoxadiazacyclotetradecine-3-carbonitrile。化学结构如下图所示:

洛拉替尼是一种白色到灰白色的粉末,pKa值为4.92。洛拉替尼在水溶液中的溶解度从32.38mg/mL降至0.17 mg/mL, pH值为2.55 ~ 8.02。pH= 9时辛醇/水的分布系数(octanol/water)的对数为2.45。
LORBRENA作为片剂提供,含有25毫克或100毫克的lorlatinib,并含有以下非活性成分:微晶纤维素、二碱性磷酸钙无水、淀粉乙醇酸钠和硬脂酸镁。该膜层包括羟丙基甲基纤维素(HPMC)2910/羟丙醇、乳糖一水化物、大环丙二醇/聚乙二醇(PEG) 3350、三乙酸乙酯、二氧化钛、氧化铁/黑氧化铁、氧化铁红。
12个临床药理学
12.1作用机理
洛拉替尼是一种激酶抑制剂,在体外对ALK和ROS1以及TYK1、FER、FPS、TRKA、TRKB、TRKC、FAK、FAK2和ACK具有活性。洛拉替尼在体外表现出对多种ALK酶突变形式的活性,包括在crizotinib和其他ALK抑制剂疾病进展时在肿瘤中检测到的一些突变。
在小鼠皮下植入含有EML4融合的ALK变体1或ALK突变的肿瘤(包括在ALK抑制剂疾病进展时在肿瘤中检测到的G1202R和I1171T突变)中,使用洛拉替尼可产生抗肿瘤活性。洛拉替尼还在eml4- alk驱动的肿瘤细胞系内移植小鼠中显示出抗肿瘤活性和延长生存期。洛拉替尼在体内模型的整体抗肿瘤活性呈剂量依赖性,并与抑制ALK磷酸化有关。
12.2药效学
关系
从研究B7461001基于数据,我们关系为3或4级高胆固醇血症和任何3或4级不良反应观察在稳态敞口达到推荐的剂量,不良反应的发生概率较高的随着lorlatinib曝光。
心脏电生理学
295例患者在B7461001研究中,每日一次以推荐剂量100mg接受洛布伦娜治疗,并进行心电图测量,PR间隔与基线的最大平均变化为16.4ms
(2侧90%上置信区间[CI] 19.4 ms)。在284例PR间隔<200ms的基线患者中,14%的患者在开始使用LORBRENA后PR间隔延长≥200ms。PR区间的延长与浓度有关。1%的患者发生房室传导阻滞。在研究B7461001的活动评估部分中,275名患者按照推荐剂量接受洛布伦纳治疗,在QTcF时间间隔中,与基线相比没有显著的平均增加(即:,>20 ms)检测。
12.3药物动力学
稳态洛拉替尼最大血浆浓度(C)成比例增加,AUC在每日一次口服10mg- 200mg剂量范围内(0.1 - 2倍推荐剂量)略低于比例增加。max在推荐剂量,意味着(变异系数(CV) %)第一名577 ng /mL(42%)和AUCwas·h 5650 ng / mL(39%)患者的癌症。max 0-24h 与单剂量相比,洛拉替尼口服清除率在稳定状态下增加,说明存在自诱导。
吸收
洛拉替尼的中位Twas为1.2小时(0.5至4小时)后,单一口服100毫克剂量和2小时(0.5至23小时)后,100毫克口服每日一次,在稳定状态。max
口服给药与静脉给药相比,平均绝对生物利用度为81% (90% CI75.7%, 86.2%)。
食物的影响
高脂肪、高热量膳食(约1000卡路里,其中150卡路里来自蛋白质,250卡路里来自碳水化合物,500至600卡路里来自脂肪)对洛雷替尼的药物动力学没有临床意义。
分布
体外,lorlatinib绑定到66%血浆蛋白的浓度2.4µM。血浆比为0.99。单次静脉给药后,平均(CV%)稳态分布体积(V)为305l(28%)。ss
消除
洛雷替尼口服100 mg后,血浆平均半衰期(t)为24小时(40%)。½单次口服100mg剂量后,平均口腔清除率(CL/F)为11L/h(35%),稳态时增至18 L/h(39%),提示存在自诱导。
新陈代谢
在体外,洛拉替尼主要由CYP3A4和UGT1A4代谢,而CYP2C8、CYP2C19、CYP3A5和UGT1A3的代谢作用较小。
在血浆中,洛拉替尼的氨基和芳香醚键氧化裂解产生的苯甲酸代谢物(M8)占人体循环放射性的21%[C]质量平衡研究。14氧化裂解代谢物M8具有药理活性。
排泄
单次口服100毫克放射性标记洛拉替尼后,48%的放射性物质在尿液中恢复(低于1%),41%的放射性物质在粪便中恢复(约9%)。
特定的人群
根据年龄(19 ~ 85岁)、性别、种族/民族、体重、轻度至中度肾功能损害(CLcr 30 ~ 89mL/min)、轻度,洛拉替尼的药代动力学无临床意义差异
肝损害(总胆红素≤ULN和AST > ULN或总胆红素>1.5×ULN和任何AST),或CYP3A5和CYP2C19代谢产物表型。中度至重度肝功能损害或严重肾功能损害对洛雷替尼药代动力学的影响尚不清楚[参见在特定人群中的应用(8.6,8.7)]。
药物相互作用研究
临床研究
CYP3A诱导剂对洛雷替尼的影响:12名健康受试者接受利福平,一种强CYP3A诱导剂,也激活PXR,每天600毫克,持续8天(第1至8天),第8天口服100毫克洛雷替尼。利福平与洛布伦那的联合用药使洛拉替尼的平均浓度降低了85%,c76%。infmax ALT或AST在3天内升高2至4级。4级ALT或AST升高50%,3级ALT或AST升高33%,2级ALT或AST升高8%。ALT和AST在7 ~ 34天内恢复到正常范围(中位15天)。同时使用中度CYP3A诱导物对洛拉替尼的药代动力学或伴随使用中度CYP3A诱导物的肝毒性风险的影响是未知的[参见药物相互作用(7.1)]。
强CYP3A抑制剂对洛雷替尼的影响:强CYP3A抑制剂伊曲康唑单次口服100mg洛雷替尼,增加auc42%,增加c24%[药物相互作用(7.1)]。infmax
洛雷替尼对CYP3A底物的影响:口服洛雷替尼150mg,每日一次,连续15天,与口服咪达唑仑(一种敏感的CYP3A底物)单次2mg剂量相比,洛雷替尼降低了auc64%,c50%[药物相互作用(7.2)]。inf max
酸还原剂对洛拉替尼的影响:同时使用质子泵抑制剂雷贝拉唑,对洛拉替尼的药代动力学没有临床意义。
体外研究
洛拉替尼对CYP酶的影响:体外研究表明,洛拉替尼是CYP3A的时间依赖性抑制剂和诱导剂,在体内激活PXR,净效应为诱导。洛拉替尼可诱导CYP2B6并激活人的雄激素受体(CAR)。洛拉替尼与主要循环代谢物M8对CYP1A2、CYP2B6、CYP2C8、CYP2C9、CYP2C19、CYP2D6均无抑制作用。M8不抑制CYP3A。
M8不诱导CYP1A2、CYP2B6和CYP3A。
洛拉替尼对udp -葡萄糖醛酸转移酶(UGT)的影响:洛拉替尼和M8对UGT1A1、UGT1A4、UGT1A6、UGT1A9、UGT2B7和UGT2B15无抑制作用。
洛拉替尼对转运体的影响:洛拉替尼抑制p糖蛋白(P-gp)、有机阳离子转运体(OCT)1、有机阴离子转运体(OAT)3、多药毒素挤出(MATE)1、肠道乳腺癌耐药蛋白(BCRP)。洛拉替尼不抑制有机阴离子转运多肽
(OATP)1B1、OATP1B3、OAT1、OCT2、MATE2K、全身BCRP。M8不抑制P-gp、BCRP、OATP1B1、OATP1B3、OAT1、OAT3、OCT1、OCT2、MATE1和MATE2K。
13 临床前毒理学
13.1 癌变、突变、生育能力下降
洛拉替尼的致癌性尚未进行研究。洛拉替尼在人淋巴母细胞样TK6细胞体外实验中为非优生药物,在大鼠骨髓中微核形成呈阳性。洛拉替尼在体外细菌反向突变(Ames)试验中没有致突变作用。
没有对洛拉替尼进行专门的生育研究。男性生殖器官的发现发生在重复剂量毒性研究中,包括睾丸、附睾和前列腺重量较低;睾丸管状变性/萎缩;前列腺萎缩;和/或附睾炎,分别为15mg/kg/d和7 mg/kg/d的大鼠和狗(分别约为8倍和2倍的人体暴露在推荐剂量为100 mg的AUC)。对男性生殖器官的影响是可逆的。
13.2动物毒理学和/或药理学
腹胀、皮疹、胆固醇和甘油三酯升高均发生于动物。这些发现是伴随着增生和扩张的胆管在大鼠肝脏和胰腺的腺泡萎缩15毫克/公斤/天,狗2毫克/公斤/天(大约8和0.5倍,分别人类接触的推荐剂量100毫克基于AUC)。在恢复期间,所有的影响都是可逆的。
14个临床研究
14.1 ALK阳性转移性非小细胞肺癌以前用ALK激酶抑制剂治疗
洛布伦纳的疗效在一组ALK阳性转移性非小细胞肺癌(NSCLC)患者中得到了证实,这些患者之前接受过一种或多种ALK激酶抑制剂治疗,这些患者参加了一项非随机、剂量范围和活性评估、多队列、多中心研究(研究B7461001;NCT01970865)。病人包括在这个小组被要求有转移性疾病至少1可衡量的目标根据响应评估标准在实体肿瘤病变(RECIST)版本1.1(v1.1), ECOG 0到2的性能状态,并记录筛选重排在肿瘤组织由荧光原位杂交(FISH)分析或通过免疫组织化学(包含IHC)和接收LORBRENA100毫克每日口服一次。无症状的中枢神经系统转移患者,包括研究开始前2周内使用稳定或减少类固醇的患者,均符合入选条件。患有包括自杀意念或自杀行为在内的严重、急性或慢性精神疾病的患者被排除在外。此外,对于alk阳性转移性非小细胞肺癌患者,每个队列都明确了既往治疗的范围和类型(见表4)。根据RECISTv1.1,主要疗效结局指标为总有效率(ORR)和颅内ORR,由独立中央审查(ICR)委员会评估。在表4中列出的所有子组中汇集了数据。其他疗效指标包括反应时间(DOR)和颅内DOR。
表4各亚组共纳入215例患者。表4按既往治疗的类型和程度列出了患者的分布情况。215例患者的人口学特征为:59%女性,51%白人,34%亚洲人,中位年龄53岁(29- 85岁),其中18%≥65岁。96%的患者在基线时的ECOG表现为0或1。所有患者均有转移性疾病,95%为腺癌。经ICR鉴定,69%的患者存在脑转移;其中,60%的患者曾接受过脑辐射,60%(n=89)在ICR中有可测量的疾病。
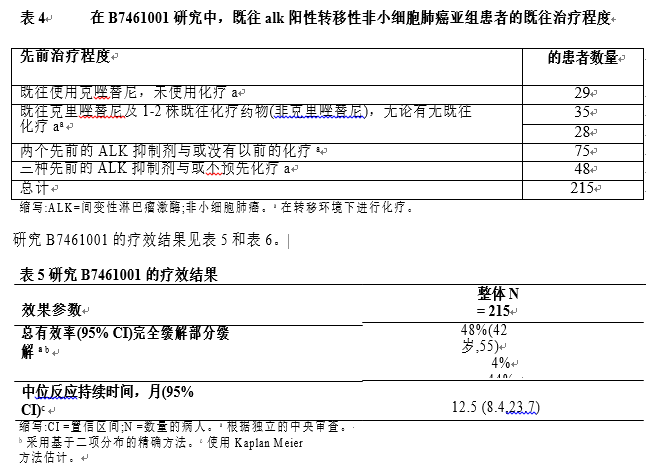
表6总结了研究B7461001中89例CNS转移患者的颅内ORR评估和CNS转移反应持续时间,这些患者的CNS基线可测量病灶根据RECISTv1.1。其中56例(63%)患者曾接受过脑放射治疗,其中42例(47%)在开始接受洛布雷纳治疗前至少6个月完成了脑放射治疗。
在以前的治疗定义的亚组中进行的探索性分析中,对LORBRENA的反应率为:
• ORR = 39% (95% CI: 30 , 119 年48 ) 病人 crizotinib 和 至少 一 个 其他ALK inhibitor, 化疗 之前 有 或 没有
• ORR = 31% (95% CI: 9 , 61 ) 在13 个 病人 alectinib 作为 他们 唯一 的ALK inhibitor, 化疗 之前 有 或 没有
• ORR = 46% (95% CI: 19 , 75 ) 在13 个 病人 ceritinib 作为 他们 唯一 的ALK inhibitor, 化疗 之前 有 或 没有
表7描述了LORBRENA的可用优势和包配置:
储存于20C至25C (68F至77F);oooo允许在15C到30C(59F到86F)之间旅行(见USP控制的室温)。oooo
17患者咨询信息
建议患者阅读fda批准的患者标识(患者信息)。
同时使用强CYP3A诱导剂有严重肝毒性的风险
告知患者同时使用强CYP3A诱导剂的潜在肝氧性风险。
建议患者告知他们的医疗保健提供者他们正在服用的所有药物,包括处方药、非处方药、维生素和草药产品(如圣约翰草)[参见警告和预防措施(5.1)]。
中枢神经系统(CNS)效应
建议患者在出现新的或恶化的中枢神经系统症状时通知他们的医疗服务提供者(参见警告和预防措施(5.2))。
高脂血症
告知患者治疗期间将监测血清胆固醇和甘油三酯。建议患者可能需要开始或增加降脂剂的剂量[参见警告和预防措施(5.3)]。
房室(AV)传导阻滞
告知病人房室传导阻滞的风险。建议患者立即与医疗服务提供者联系,报告新的或恶化的心脏症状[参见警告和预防措施(5.4)]。
间质性肺病(ILD)/肺炎
告知患者严重ILD/肺炎的风险。建议患者立即与医疗服务提供者联系,报告新的或恶化的呼吸道症状[参见警告和预防措施(5.5)]。
胎儿毒性
告知女性胎儿的潜在生殖风险。建议女性将已知或疑似怀孕的情况通知她们的卫生保健提供者(参见警告和预防措施(5.6),用于特定人群(8.1))。
建议有生育潜力的女性在接受洛布伦娜治疗期间和最后一次使用洛布伦娜后至少6个月期间使用有效的非激素避孕措施(见特定人群使用情况(8.3))。
建议有生育潜力的女性伴侣的男性患者在使用LORBRENA治疗期间和最终剂量后至少3个月使用有效的避孕措施[参见特定人群使用(8.3),非临床毒理学(13.1)]。
泌乳
建议妇女在使用LORBRENA治疗期间和最后剂量后7天内不要母乳喂养(见特定人群使用情况(8.2))。
不孕不育
建议男性注意LORBRENA可能会暂时影响生育能力的生殖潜能[参见在特定人群中的使用(8.3),非临床毒理学(13.1)]。
这个产品的标签可能已经更新了。欲了解完整的处方信息,请访问www.LORBRENA.com。

