批准日期: 2017年3月23日;公司:Shionogi Inc.
为治疗:阿片诱导便秘
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/208854s000lbl.pdf
处方资料重点
这些重点不包括安全和有效使用SYMPROIC需所有资料。请参阅SYMPROIC完整处方资料。
SYMPROIC®(naldemedine)片,为口服使用,C-II 、
美国初次批准:2017
适应证和用途
SYMPROIC是一种阿片拮抗剂适用为阿片诱导便秘(OIC)在有慢性非-癌痛成年患者的治疗(1)
剂量和给药方法
给药(2.1):
●SYMPROIC开始前不需要另外镇痛给药方案的改变。
●患者接受阿片类共少于4周可能对SYMPROIC较低反应。
● 终止SYMPROIC如治疗用阿片疼痛药物剂量也被终止。(2.2):
● 在成年找,推荐剂量为0.2 mg每天1次有或无食物
剂型和规格
片:0.2 mg naldemedine(3)
禁忌证
●患者有已知怀疑胃肠道阻塞或处于复发阻塞风险增加。(4,5.1)
●患者有对naldemedine超敏性反应的病史(6.1)
警告和注意事项、
● 胃肠道穿孔:在有已知或怀疑GI道病变患者考虑总体风险获益。对严重,持续,或恶化的腹痛监视:如症状发展终止(5.1)
● 阿片类戒断综合征:在有对血脑屏障障碍患者考虑总体风险获益。监视阿片类戒断综合征的症状。(5.2)
不良反应
最常见不良反应(≥2%)为:腹痛,腹泻,和恶心。(6.1)
报告怀疑不良反应,联系Shionogi Inc.电话1-800-849-9707或FDA电话1-800-FDA-1088或www.fda.gov/medwatch.
药物相互作用
● 强CYP3A诱导剂(如,利福平[rifampin]):减低naldemedine浓度:避免同时使用(7)
● 其他阿片拮抗剂:对增加相加作用和阿片类戒断综合征风险潜能:避免同时使用(7)
● 中度(如,氟康唑)和强(如,伊曲康唑[itraconazole]) CYP3A4抑制剂:增加naldemedine浓度:监视对不良反应。(7)
● P-gp抑制剂(如,环孢霉素[cyclosporine]):监视对不良反应。(7)
在特殊人群中使用
●妊娠:可能促进在胎儿中阿片类戒断综合征。(8.1)
●哺乳:终止药物或哺乳喂养考虑药物对母亲的重要性。(8.2)
●肝受损:在严重损伤中避免。(8.7)
完整处方资料
1 适应证和用途
SYMPROIC是适用为有慢性非-癌痛成年患者阿片诱导便秘(OIC)的治疗。
2 剂量和给药方法
2.1 给药
● 开始SYMPROIC前不需要镇痛给药方案的改变。
●患者接受阿片类共少于4周对SYMPROIC反应可能较低。[见临床研究(14)].
● 终止SYMPROIC如治疗用阿片疼痛药物也被终止。
2.2 成年剂量
SYMPROIC的推荐剂量是0.2 mg口服每天1次有或无食物。
3 剂型和规格
片:0.2 mg naldemedine:以黄色,圆形,膜包衣,凹陷有Shionogi 标记上鉴定码222在一侧和在其他侧0.2供应。
4 禁忌证
SYMPROIC在以下禁忌:
●患者有已知或怀疑胃肠道阻塞和处于复发阻塞风险增加患者,由于对胃肠道穿孔潜能[见警告和注意事项(5.1)]。
●患者对naldemedine超敏性反应病史。有包括支气管痉挛和皮疹反应[见不良反应(6.1)].
5 警告和注意事项
5.1 胃肠道穿孔
另一种外周作用阿片拮抗剂的使用曽报告胃肠道穿孔病例在患者有情况可能伴随有局部化或胃肠道壁中结构完整性的弥漫减低的使用(如,消化性溃疡疾病,Ogilvie氏综合证,憩室病,浸润性消化道恶性肿瘤,或腹膜转移)。在有这些情况患者或其他情况可能导致胃肠道壁完整性受损(如,克罗恩病)中当使用SYMPROIC考虑总体风险-获益图形。对严重,持久性,或恶化的腹痛监视发展:发生这个症状患者中终止SYMPROIC[见禁忌证(4)]。
5.2 阿片类戒断综合征
在用SYMPROIC治疗患者中曽发生症状的集群与阿片类戒断综合征一致,包括多汗症,发冷,增加流泪,脸面热发红[hot flush/flushing],发热,打喷嚏,感觉冷,腹痛,腹泻,恶心,和呕吐[见不良反应(6.1)]。
患者有对血脑屏障混乱[disruptions]可能是处于对阿片类戒断综合征或镇痛减低风险增加。在这类患者中使用SYMPROIC时考虑总体风险-获益图形。在这类患者中监视对阿片类戒断综合征的症状。
6 不良反应
在说明书其他处描述严重和重要不良反应包括:
● 胃肠道穿孔[见警告和注意事项(5.1)]
● 阿片类戒断综合征[见警告和注意事项(5.2)]
6.1 临床试验经验
因为临床试验是在广泛不同情况下进行的,临床试验观察到不良反应率不能与另一种药临床试验发生率直接比较而且可能不反映实践中观察到的发生率。
下面所述数据反映在临床试验在1163患者对SYMPROIC暴露,包括487患者有暴露大于6个月和203患者有暴露12个月。
以下安全性数据是来自三项双盲,安慰剂-对照试验在患者有OIC和慢性非-癌痛:两项12-周研究(研究 1和2)和一项52-周研究(研究3)[见临床研究(14)]。
在研究1和2,患者用泻药被要求终止研究纳入前他们的使用。4在研究期间所有患者被限制至比沙可啶抢救治疗。在研究3中,在两治疗组约60%的患者在基线是用一个泻药方案;研究时间自始至终患者被允许继续使用他们的泻药方案。SYMPROIC的安全性图形相对于安慰剂是相似不管使用泻药。
表1和2列出常见不良反应发生在至少2%的患者接受SYMPROIC和在一个发生率大于安慰剂。表1显示来自研究1和2合并的12-周数据。表2显示来自研究3的12-周数据。
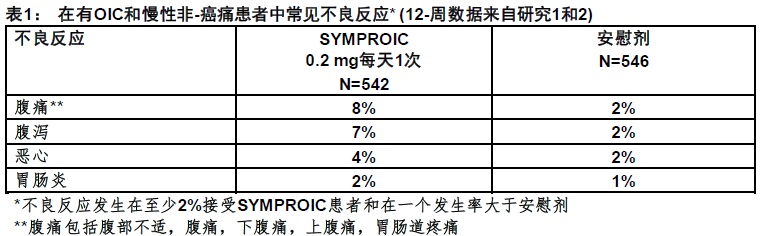
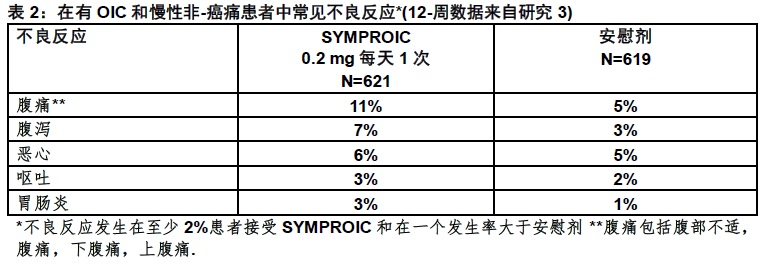
在研究3在不良反应至12个月是相似于那些列出在表1和2对SYMPROIC和安慰剂分别(腹泻:11%相比较5%,腹痛:8%相比较3%,和恶心:8%相比较6%)。
阿片类戒断综合征
在研究1,2和3,为根据研究者评估不良反应与阿片类戒断综合征一致和判断根据至少3个不良反应的发生潜在地与阿片类戒断综合征相关在同一个在同一个群集[constellation]发病发病那些症状发生在相同天或彼此的在一天内。.
阿片类戒断综合征不良反应的可能性可能包括非-胃肠道(GI)症状(如,多汗症,热脸红或脸红,发冷,振颤,心动过速,焦虑,激动,打呵欠,鼻液溢,增加流泪,打喷嚏,感觉冷,和发热), GI症状(如,呕吐,腹泻,或腹痛),或GI和非-GI症状两者。.
在合并研究1和2中,阿片类戒断综合征不良反应的发生率对SYMPROIC为1%(8/542)和对安慰剂为1%(3/546)。在研究3(52-周数据),对SYMPROIC发生率为3%(20/621)和对安慰剂为1%(9/619)。大多数SYMPROIC治疗受试者经受接近等同仅GI或GI和非-GI症状两者发生率。
较不常见不良反应:
两例患者在一个单次剂量的SYCMPROI发生超敏性的症状。一例患者报告支气管痉挛和另一例皮疹。
7 药物相互作用
表3包括药物与SYMPROIC有临床上重要药物相互作用和指导为预防或处理相互作用。
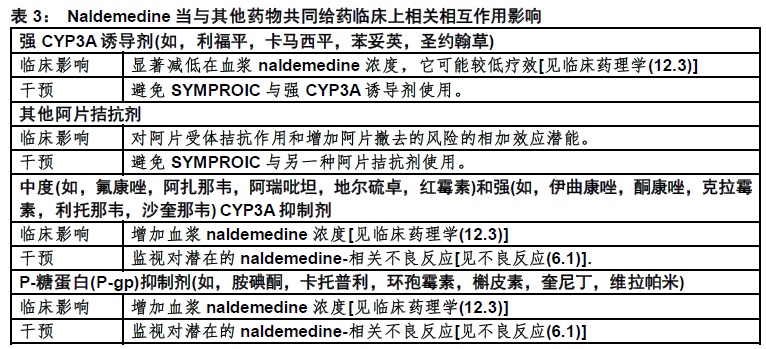
8 在特殊人群中使用
8.1 妊娠
风险总结
没有在妊娠妇女中用naldemedine可得到的数据告知药物-关联重大出生缺陷和流产的风险。. 当在妊娠妇女中使用SYMPROIC在胎儿中有对阿片类戒断综合征潜能[见临床考虑]。妊娠期间仅如潜在获益胜过潜在风险时SYMPROIC才应被使用。
在一个大鼠胚胎-胎儿发育研究中在器官形成阶段期间口服给予naldemedine在剂量导致人血浆浓度时间曲线下面积(AUC)在推荐人剂量0.2 mg/day全身暴露约23,000倍时,未观察到发育异常。在兔中在器官形成阶段口服给予naldemedine在剂量导致全身暴露约226倍人AUC在推荐人剂量0.2 mg/day,对胎儿发育没有不良影响[见数据]。在大鼠在暴露12倍人暴露在推荐人剂量时未观察到围产期发育的影响。
不知道对适应证人群重大出生缺陷和流产的估算背景风险。所有妊娠有一个出生缺陷,丢失,或其他不良结局。在美国一般人群,重大出生缺陷和在临床上认可妊娠的流产估算的背景风险分别是2至4%和15至20%。
临床考虑
胎儿/新生儿不良反应
Naldemedine跨越胎盘,和可能在胎儿中促进阿片类戒断综合征由于不成熟的胎儿血-脑屏障。
数据
动物数据
在大鼠中,在器官形成阶段期间在口服给予naldemedine剂量至1000 mg/kg/day(约23,000倍推荐人剂量时人暴露(AUC))时,对胚胎-胎儿发育无不良影响。在兔中,在器官形成阶段期间口服给予naldemedine在剂量至100 mg/kg/day(约226倍推荐人剂量时人 暴露(AUC))对胚胎-胎儿发育无不良影响。在400 mg/kg/day(约844倍推荐人剂量时人暴露(AUC)),在母体动物的影响包括体重减轻/减低体重增量和食物耗量,胎儿丢失,和早产减低胎儿体重在这个剂量可能是与观察到的母体毒性相关。在围产期发育研究,妊娠大鼠被给予naldemedine 在口服剂量至1000 mg/kg/day从妊娠天7至哺乳天20。在大鼠在1 mg/kg/day(约12倍推荐人剂量时人暴露(AUC)),未观察到围产期发育的影响。一只单个母收在分娩时死亡在1000 mg/kg/day,和减低体重/体重增量和食物耗量,差营养,和总窝丢失被注意到在30和1000 mg/kg/day(分别约626和17,000北推荐人剂量时人暴露(AUC))。在天4子代活力指数减在30和1000。被注意到在30和1000 mg/kg/day在出生后天4子代活力指数减低,注意到在1000 mg/kg/day幼崽中 和低体重和幼崽耳廓延迟展开。
8.2 哺乳
风险总结
没有信息关于在人乳汁中naldemedine的存在,对哺乳喂养婴儿的影响,或对乳汁产生的影响。Naldemedine是存在在大鼠乳汁中[见数据]。因为对在哺乳喂养婴儿做对严重的不良反应潜能,包括阿片类戒断综合征。因为在哺乳喂养婴儿中对严重的潜能,应做出决定终止哺乳喂养或终止药物考虑到药物对母亲的重要性。如果药物被终止为了最小药物暴露至一例哺乳喂养婴儿,建议妇女哺乳喂养可在SYMPROIC最后剂量后3天恢复哺乳喂养。
数据
在单次口服剂量药物1 mg/kg[羰基-14C]-naldemedine -相关放射性是转移至哺乳大鼠。
8.4 儿童使用
未曽确定在儿童患者中SYMPROIC的安全性和有效性。
8.5 老年人使用
在临床研究暴露至SYMPROIC的1163患者中,183(16%)为65岁和以上,而37(3%)为75 岁和以上。这些和较年轻患者间被观察到在安全性或有效性无总体差别,但不能除外有些老年个体更大敏感度。在一项群体药代动力学分析,未观察到naldemedine药代动力学年龄-相关改变(12.3)]. 。
8.6 肝受损
未评价严重的肝受损(Child-Pugh类别C)对naldemedine的药代动力学。在有严重的肝受损患者中避免使用SYMPROIC。在有轻度或中度肝受损患者中无需调整SYMPROIC剂量[见临床药理学(12.3)].
9 药物成瘾和依赖性
9.1 受控物质
SYMPROIC含naldemedine,一种附表二受控物质.
10 药物过量
在临床研究中单次剂量naldemedine至00 mg(500倍推荐剂量)和多次剂量至30 mg(150倍推荐剂量)共10天曽被给予健康受试者。观察到剂量-依赖增加在胃肠道-相关不良反应,包括腹痛,腹泻,和恶心。单次剂量的naldemedine至3 mg(15倍推荐剂量)和多次剂量的 0.4 mg(两倍推荐剂量共28天曽给予至患者有OIC在临床探究中。观察到在胃肠道-相关不良反应依赖剂量增加,包括腹痛,腹泻,恶心,和呕吐。还有,发冷,多汗症,和眩晕被报道在在 1和3 mg剂量更频和多汗症在0.4 mg剂量。对naldemedine无已知抗毒药。血液透析不是有效措施从血液去除naldemedine[见临床药理学(12.3)]。
11 一般描述
SYMPROIC(naldemedine),一个阿片拮抗剂,含naldemedine甲苯磺酸盐作为活性成分。Naldemedine甲苯磺酸盐的化学名是:17-(cyclopropylmethyl)-6,7-didehydro-4,5α-epoxy3,6,14-trihydroxy-N-[2-(3-phenyl-1,2,4-oxadiazol-5-yl)propan-2-yl]morphinan-7-carboxamide 4-methylbenzenesulfonic acid。结构式是:
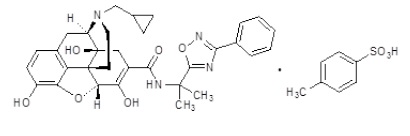
对naldemedine甲苯磺酸盐的经验式为C32H34N4O6•C7H8O3S和分子量为742.84。Naldemedine甲苯磺酸盐是白色至浅褐色粉末,溶于二甲基亚砜和甲醇,略微溶于乙醇和水,和pH无关。SYMPROIC(naldemedine)片为口服使用含0.2 mg naldemedine(等同于0.26 mg的naldemedine甲苯磺酸盐),赋形剂是:D-甘露醇,交联羧甲纤维素钠,硬脂酸镁,羟丙甲纤维素,滑石,和黄色氧化铁.
12 临床药理学
12.1 作用机制
Naldemedine是一种阿片拮抗剂对µ[mu]-,δ[delta]-,和κ[kappa\-阿片受体的结合亲和力。Naldemedine功能如同一个在组织中外周-作用µ-阿片受体拮抗剂例如胃肠道,因此减低阿片的便秘效应。
Naldemedine是纳曲酮[naltrexone]的衍生物对它已被加上侧链,它增加分子量和极性表面积,因此减低它跨越血脑屏障(BBB)的能力。Naldemedine也是P-糖蛋白(P-gp)流出转运蛋白的底物。根据这些性质,naldemedine的中枢神经系统CNS穿透预计在推荐剂量水平是可忽略不计,限制与对中枢介导阿片镇痛干扰。
12.2 药效动力学
阿片类的使用诱导胃肠道运动和传递的减慢。胃肠道µ-阿片受体的拮抗作用被naldemedine抑制阿片-诱导延迟胃肠道通过时间。对心脏复极化作用在剂量至5-倍推荐剂量,SYMPROIC不延长QT间期至任何临床上相关程度。
12.3 药代动力学
吸收
在空腹状态中口服给药后,naldemedine被吸收有达峰浓度时间(Tmax)约0.75小时。跨越被评价剂量范围,最高血浆浓度(Cmax)和浓度时间曲线下面积(AUC)在剂量正比例方式或几乎剂量-正比例方式。在naldemedine多次每天给药后积蓄小。
食物影响
一个高-脂肪餐减低率,但不是naldemedine吸收的程度。Cmax是减低约35%和到达Cmax时间是延迟从在空腹状态0.75 小时至进食状态2.5小时,而在进食状态AUC没有意义的变化[见剂量和给药方法(2.2)]。
分布
Naldemedine在人中的血浆蛋白结合是93%至94%。末端相时均数表观分布容积(Vz/F)是155 L。
消除
Naldemedine的末端消除半衰期是11小时。
代谢
Naldemedine是主要地被CYP3A代谢为去甲-naldemedine,与次要贡献来自UGT1A3形成aldemedine 3-G。去甲-naldemedine和naldemedine 3-G曽被显示有拮抗活性对阿片受体,比naldemedine效力较低。[14C]-标记的naldemedine的口服给药后,血浆主要代谢物是去甲naldemedine,与naldemedine比较一个相对暴露为其约9%至13%。在血浆中Naldemedine 3-G是一个次要代谢物,有一个相对暴露为naldemedine的低于3%。 Naldemedine在GI道中还进行裂解形成benzamidine和naldemedine羧酸。
排泄
[14C]-标记的naldemedine的口服给药后,在尿和份中排泄的放射性总量分别为naldemedine给药剂量的57%和35%。在尿中排泄未变化naldemedine的量是给药剂量的约16%至18%。Benzamidine是在尿和粪排泄的最优势代谢物,分别代表naldemedine给药剂量的约32%和20%。未曽确定未变化药物在份中的百分率。
在特殊人群中使用
年龄:老年人群,性别,种族/民族
来自临床研究用naldemedine一项群体药代动力学分析没有鉴定年龄,性别,或种族对naldemedine药代动力学一个临床上意义影响。
肾受损
给予0.2 mg单次口服剂量SYMPROIC后研究naldemedine的药代动力学,在8受试者有轻(n=8,估算的肾小球滤过率[eGFR] 60至89 mL/min/1.73 m2),中度(n=8,eGFR 30至59 mL/min/1.73 m2),和严重(n=6,eGFR低于 30 mL/min/1.73 m2)肾受损,和受试有有肾病终末期(ESRD)需要血液透析(n=8),和有正常肾功能健康受试者比较(n=8,估算的肌酐清除率至少90 mL/min)。在所有组中受试者间naldemedine的药代动力学相似。有ESRD需要血液透析受试者中当 SYMPROIC被给予或血液透析前-或后naldemedine的血浆浓度是相似,表明naldemedine是不被血液透析从血液去除。
肝受损
在受试者有肝受损被分类为轻度(n=8,Child-Pugh类别A)或中度(n=8,Child-Pugh 类别B)中研究肝受损对0.2 mg单次口服剂量SYMPROIC药代动力学的影响和与有正常肝功能健康受试者(n=8)比较。在所有组中受试者间naldemedine的药代动力学相似。未评价严重肝受损(Child-Pugh类别C)对naldemedine的药代动力学的影响[见在特殊人群中使用(8.6)]。
药物相互作用研究
Naldemedine对其他药物的影响
在体外研究在临床上相关浓度,naldemedine不抑制主要CYP酶(包括CYP1A2,CYP2A6,CYP2B6,CYP2C8,CYP2C9,CYP2C19,CYP2D6,CYP2E1,CYP3A4/5,或CYP4A11 同工酶)和不是转运蛋白的抑制剂(包括OATP1B1,OATP1B3,OCT1,OCT2,OAT1,OAT3,BCRP,或P-gp)。Naldemedine不致CYP1A2,CYP2B6,CYP3A4,UGT1A2,UGT1A6,或UGT2B7同工酶的显著抑制作用。
其他药物对Naldemedine的影响
Naldemedine是主要地被CYP3A4酶代谢有次要贡献来自UGT1A3。Naldemedine是一个P-gp的底物。图1总结了共同给药药物对naldemedine的药代动力学的影响。
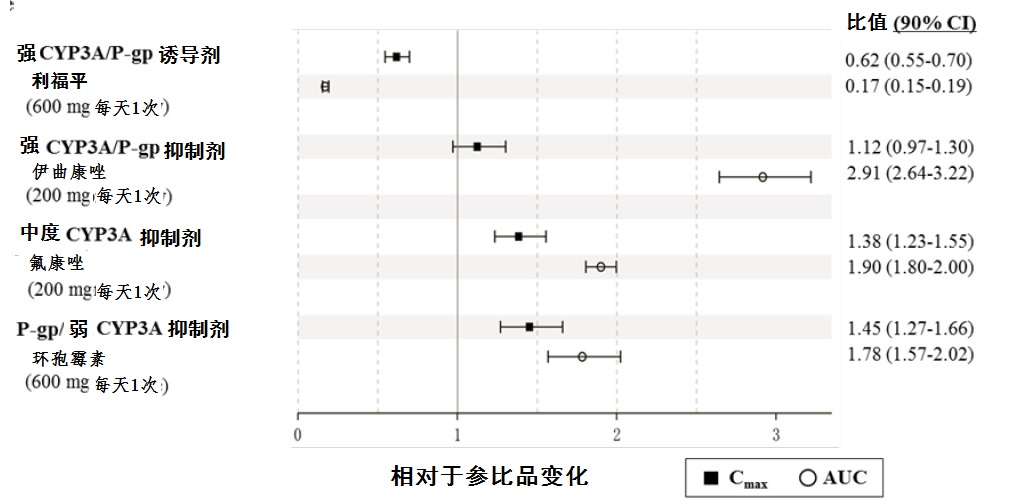
图1:共同给药药物对Naldemedine的药代动力学的影响
Efavirenz(中度CYP3A诱导剂):利用基于生理学的药代动力学模型分析模拟提示efavirenz的同时使用减低对naldemedine的暴露43%。不知道这个减低暴露的临床后果。未曽进行对SYMPROIC与药物改变胃pH(如,抗酸药,质子泵抑制剂)药物相互作用研究。
13 非临床毒理学
13.1 癌发生,突变发生,生育力受损
癌发生
在2-年致癌性研究中,口服给予naldemedine至小鼠和大鼠在剂量至100 mg/kg/day(在推荐人剂量时人暴露(AUC)没有药物-相关肿瘤发现分别约17,500和6,300倍)。
突变发生
Naldemedine不是遗传毒性在体外细菌回复突变(Ames)试验,一个用培养中国仓鼠肺细胞染色体畸变试验,和一个用大鼠骨髓细胞体内微核试验。
生育力受损
在雄性和雌性大鼠在口服剂量至1000 mg/kg/day(在推荐人剂量时人暴露(AUC)约17,000倍Naldemedine被发现对生育力或对生殖性能无影响。在雌性大鼠,在10 mg/kg/day(在推荐人剂量时人暴露(AUC)约179倍)注意到间情期的延长。.
14 临床研究
在两项重复,12-周,随机化,双盲,安慰剂-对照试验(研究1和研究2)其中SYMPROIC被使用无 泻药在有OIC和慢性非癌疼痛患者评价SYMPROIC。
在纳入前患者接受一个稳定的阿片吗啡等同物每天剂量至少30 mg共至少4周和自我报告的OIC是合格的对临床试验参加者。
患者胃肠道有显著结构性异常的证据是不被纳入这些试验。
在研究1和2,患者在筛选和治疗阶段时曽或被不使用泻药或愿意终止泻药使用和愿意仅使用提供的抢救泻药。
在研究1和2,通过2周磨合阶段确证OIC和被定义为不超过4次自发的肠运动(SBMs)总共历时14连续天和少于3次SBMs在一个给定周有至少25%的SBMs伴随一次或更多以下情况:(1) 拉紧变形[straining]:(2) 硬或块状粪便[lumpy stools]:(3) 有不完全排空的感觉;和(4) 有肛门直肠堵塞的感觉。
一次SBM被定义为一次肠道运动(BM)在过去24小时内没有用泻药抢救。患者历时7连续天和2周筛选阶段期间无BMs和前或患者从未服用泻药患者被排除。
在筛选和治疗阶段,比沙可啶[bisacodyl]被使用作为抢救泻药如患者未曽有一个BM共72小时和被允许一次使用的灌肠剂,如服用比沙可啶后24小时他们仍没有一次BM.
在研究1总共547患者和在研究2中553患者被随机化以一个1:1比值接受SYMPROIC 0.2 mg每天1次或安慰剂共12周。研究药物是给予不考虑进餐。
在研究1和2受试者均数年龄为54岁:59%为女性;和80%为白种人。在研究1和2的最常见疼痛类型为背或颈痛(61%)。对研究1和2SBMs的基线数的均数为1.3和1.2每周。
纳入前,患者正在使用他们的当前阿片共中位时间约5年。被使用宽广范围的阿片类。均数基线阿片吗啡等同物每天剂量对研究1和2分别为132 mg和121 mg每天。.
在研究 1和2用一个反应者分析评估SYMPROIC的疗效。一个反应者被定义为一名患者他有至少3次SBMs每周和一个从基线变化至少1次SBM每周共至少9/12周和3/4最后周在研究1和2.
在表4中显示研究1和2中反应者率。
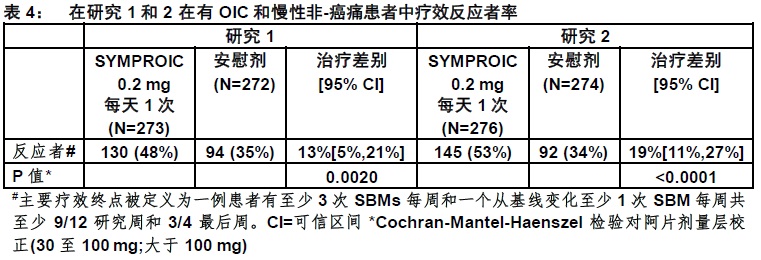
在研究1和2中,SBMs每周从基线至12-周治疗阶段的最后2周的频数这均数增加分别为3.1对SYMPROIC相比较对安慰剂2.0(差别1.0,95% CI 0.6,1.5),和3.3对SYMPROIC相比较对安慰剂2.1(差别1.2,95% CI 0.8,1.7)。
治疗阶段的周1,SBMs的频数每周从基线中均数增加对SYMPROIC为3.3相比较1.3 对安慰剂为(差别 2.0,95% CI 1.5,2.5)在研究1和在研究2对SYMPROIC为3.7相比较对安慰剂1.6(差别 2.1,95% CI 1.5,2.6)。
在研究1中,对SYMPROIC完成SBM(CSBM)每周的频数中从基线至12-周治疗阶段的最后2周均数增加为2.3相比较对安慰剂为1.5(差别0.8,95% CI 0.4,1.2)和在研究2中,对SYMPROIC为2.6相比较对安慰剂为1.6(差别1.1,95% CI 0.6,1.5). 。一个CSBM被定义为一次SBM伴随完全排空的感觉。在研究1对SYMPROIC无拉紧变形[straining]每周SBM2s的频数中从基线至治疗阶段的最后2周 的变化为1.3相比较对安慰剂为0.7(差别 0.6,95% CI 0.2,0.9)和在研究2中,对SYMPROIC为1.8相比较对安慰剂为1.1(差别0.7,95% CI 0.3,1.2)。
16 如何供应/贮存和处置
SYMPROIC是以0.2 mg naldemedine片供应在90片瓶中 - NDC 59011-523-90。
贮存SYMPROIC在抗光容器在20至25°C(68至 77°F):外出允许至15至30°C(59至86°F)[见USP控制室温]。
17 患者咨询资料
建议患者阅读FDA-批准的患者说明书(用药指南)。
给药
建议患者终止SYMPROIC如治疗用阿片疼痛药物是也被终止。
胃肠道穿孔
建议患者如他们发生不寻常地眼中,持续或恶化的腹痛终止SYMPROIC和及时寻求医学关注[见警告和注意事项(5.1)]。
阿片类戒断综合征
忠告患者服用SYMPROIC可能发生症状的群集与阿片类戒断综合征一致和如症状发生联系他们的卫生保健提供者[见警告和注意事项(5.2)]。
妊娠
建议生殖潜能女性,她成为妊娠或正在计划成为妊娠,妊娠期间使用SYMPROIC during 妊娠可能促进在胎儿中阿片类戒断综合征由于未发育的血-脑屏障[见在特殊人群中使用(8.1)]. 哺乳
建议哺乳喂养妇女,在SYMPROIC治疗期间和最后剂量后共3天内建议不要哺乳喂养[见在特殊人群中使用(8.2)]。

